Historie vědy: Vědci používají „chemii kliknutí“ ke sledování molekul v živých organismech — 23. října 2007
RYCHLÉ FAKTA
Milník: Vědci vyvinuli chemický recept na sledování molekul v živých tvorech
Datum: 23. října 2007
Kde: Kalifornská univerzita, Berkeley a další laboratoře
SZO: Tým vědců pod vedením Carolyn Bertozzi
V roce 2007 vědci publikovali papír který stanovil recept na nový typ biochemie. Metoda by vědcům umožnila vidět, co se děje v organismech v reálném čase.
Glykany jsou jednou ze tří hlavních tříd biomolekul (vedle proteinů a nukleových kyselin) a byly podílí se na zánětech a onemocněníchale vědci zjistili, že je obtížné je vizualizovat. Aby tak učinil, Bertozzi stavěl na chemickém přístupu, který propagovali biochemici K. Barry Sharpless ze Scripps Research a Morten Meldal z univerzity v Kodani.
Sharpless položil a vize pro „klikací chemii“ — způsob, jak rychle vytvořit složité biologické molekuly spojením menších podjednotek.
Biologické molekuly mají často vázané páteře uhlík atomy, ale atomy uhlíku se nechtějí spojovat. To znamenalo, že historicky museli chemici používat pečlivé, vícestupňové procesy, které využívaly více enzymů a zanechávaly nežádoucí vedlejší produkty. To bylo v pořádku pro laboratoř, ale špatné pro hromadnou výrobu biomolekul pro léčiva.
Sharpless si uvědomil, že by mohli tento proces zjednodušit a rozšířit, pokud by dokázali spojit jednoduché molekuly, které již měly kompletní karbonový rám. Potřebovali jen rychlý, výkonný a spolehlivý konektor.
Odděleně došlo k Sharplessovi a Meldalovi na kritickém konektoru: chemické reakci mezi sloučeninami azidem a alkynem. Trik spočíval v přidání mědi jako katalyzátoru.
The reakce byl extrémně silný a rychlý a došlo k němu více než 99,9 % té doby, aniž by produkovaly nějaké vedlejší produkty.
Ale pro Bertozziho nastal problém: měď je pro buňky vysoce toxická.
Bertozzi tedy pročesával literaturu, aby vymyslel klikací chemii, která by byla bezpečná v živých buňkách. Odpověď našla v desetiletí staré práci: Azid a alkyn by reagovaly „výbušně“, bez potřeby katalyzátoru, pokud by byl alkyn nucen získat prstencový tvar.
V roce 2004 to její tým prokázal tato reakce by mohla být použita k připojení molekul azidu k živým buňkám aniž by jim ublížil. A v roce 2007 Bertozzi a kolegové použili její metodu k vizualizaci glykanů v živých křeččích buňkách.
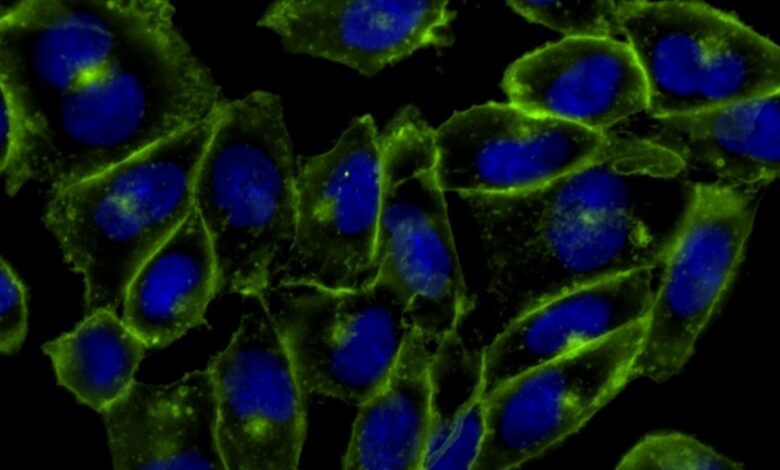
Její proces zahrnoval začlenění molekuly sacharidu modifikovaného azidem do glykanů v živých buňkách. Když přidali alkynovou molekulu ve tvaru prstence, která byla navázána na zelený fluorescenční protein, azid a alkyn se spojily a zářící zelený protein odhalil, kde jsou glykany v buňce.
Bertozzi nazval proces „bioortogonální“ klikací chemie – tak pojmenován proto, že by byl ortogonální k – to znamená, že by nezasahoval – do biologických procesů probíhajících v buňce. Její práce se ukázala jako zásadní pro pochopení toho, jak se malé molekuly pohybují živými buňkami. Bylo použito ke sledování glykany v zebřičkách embrya, abyste viděli jak rakovinné buňky se označují za bezpečné před imunitním útokem pomocí molekul cukrua vyvinout radioaktivní „stopovačky“ pro biomedicínské zobrazování. A klikací chemie v širším měřítku proces přeplňovala objev drog.
V roce 2022 Sharpless, Meldal a Bertozzi získali Nobelovu cenu za chemii za práci na chemii kliknutí.