Výpočetní hluboký ponor odhaluje skryté cíle léků na rakovinu a příležitosti k přepracování
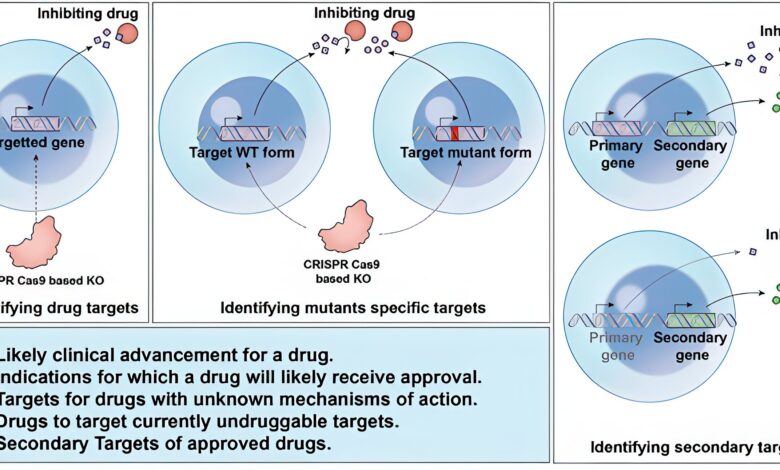
Předpovědi DeepTarget jsou založeny na principu, že odstranění genu kódujícího proteinový cíl daného léku pomocí úpravy genu CRISPR-Cas9 může napodobit inhibiční účinky tohoto léku. Tento nástroj byl vytvořen využitím rozsáhlých experimentů s genetickým a screeningem léků s komplexními daty pro 1450 léků napříč 371 rakovinnými buněčnými liniemi. Kredit: Sanju Sinha, Sanford Burnham Prebys
Podle nové studie zveřejněné 5. npj Přesná onkologie.
„Druhy malé molekuly reprezentující mnoho našich léků se v přírodě vyskytuje jen zřídka, takže se nevyvinuly k provádění konkrétního úkolu,“ řekl Sanju Sinha, Ph.D., odborný asistent v programu Cancer Metabolism and Microenvironment Program v Sanford Burnham Prebys Medical Discovery Institute. „Někdy se pole dívá na tyto léky s tunelovým viděním z hlediska toho, že mají jeden cíl jako offtar“ spolu s některými vedlejšími účinky.“
„Holističtější pohled odhaluje, že malé molekuly mohou mít různé cíle a účinky v závislosti na onemocnění a typu buňky a my můžeme tyto znalosti využít k tomu, abychom více léků použili k léčbě více pacientů.“
DeepTarget předpovídá účinky léků
Počínaje během svého tréninku v National Cancer Institute zkoumal Sinha tvárnost léků s malou molekulou vyvinutím výpočetního nástroje nazvaného DeepTarget. Spíše než se spoléhat na chemické struktury léků, Sinha a jeho spolupracovníci použili data z rozsáhlých genetických a lék screeningové experimenty na rakovinných buňkách. Jejich datový soubor zahrnoval komplexní údaje o 1450 drogách z 371 rakovinné buněčné linie z Mapa závislostí (DepMap) Snaha konsorcia vytvořit atlas rakovinových zranitelností.
V sedmi z osmi testů porovnávajících výpočetní předpovědi primárních cílů léků proti rakovině s existujícími údaji o párech lék-cíl si DeepTarget vedl lépe než současné nejmodernější nástroje včetně RoseTTAFold All-Atom a Chai-1. Výzkumný tým také prokázal, že DeepTarget může předpovědět, zda léky mají preferenční účinky na typické, nemutované cílové proteiny nebo jejich mutantní formy, a také určit sekundární cíle léků.
Vědci porovnali schopnost DeepTarget předpovídat sekundární cíle porovnáním jeho výkonu s existujícími údaji o 64 lécích proti rakovině, o kterých je známo, že mají více než jeden cíl.
„Schopnost předvídat tyto sekundární cíle je důležitá, protože mnoho léků schválených FDA a nových léků v klinickém vývoji je má,“ řekl Sinha, hlavní autor rukopisu. „Pokud je budeme vnímat spíše jako funkce než jako chyby, můžeme tyto cíle využít ke zlepšení přeměny léčiv.“
Případová studie: Nečekaný cíl Ibrutinibu
Aby výzkumný tým potvrdil svá zjištění, provedl dvě experimentální případové studie, včetně jedné o Ibrutinibu, léku na rakovinu krve schváleném FDA. Předchozí klinický výzkum ukázal, že Ibrutinib může léčit rakovinu plic, i když primární cíl léku – protein zvaný Brutonova tyrozinkináza (BTK) – není v plicních nádorech přítomen.
Ve spolupráci s laboratoří spoluodpovídající autorky Ani Deshpande, Ph.D., profesorky v programu Cancer Genome and Epigenetics Program v Sanford Burnham Prebys, vědci testovali předpověď DeepTarget, že Ibrutinib zabíjí. rakovina plic buňky působením na sekundární cílový protein nazývaný receptor epidermálního růstového faktoru (EGFR).
„Pokud jsme se při konzultaci s DeepTarget zaměřili pouze na krevní nádory, pak byl BTK primárním cílem,“ řekl Sinha. „Pokud jsme změnili naše zaměření na solidní nádory, pak se primárním cílem stala mutantní, onkogenní forma EGFR, takže to byl jasný příklad kontextově specifického cíle.“
Vědci porovnávali účinky Ibrutinibu na rakovinné buňky s rakovinným mutantem EGFR a bez něj. Buňky obsahující mutantní formu byly citlivější na lék, což potvrdilo EGFR jako cíl ibrutinibu.
Důsledky pro vývoj a přeměnu léčiv
„Věříme, že vynikající výkon tohoto nástroje v reálných scénářích je způsoben tím, že věrněji odráží skutečné mechanismy léčiv, kde buněčný kontext a účinky na úrovni dráhy často hrají zásadní roli nad rámec přímých vazebných interakcí,“ řekl Sinha.
„Také podtrhuje potenciál DeepTarget urychlit vývoj léků a úsilí o nové využití jako doplňkový přístup vedle strukturálních metod zaměřených na chemickou vazbu.“
Do budoucna chce Sinha stavět na tom, co se tým naučil, aby vytvořil nové kandidátní léky s malou molekulou.
„Potenciální zásoba chemikálií je mnohem větší, než jsme schopni provést screening i pomocí moderních, vysoce výkonných metod screeningu léků,“ řekl Sinha.
„Zlepšování možnosti léčby u rakoviny a souvisejících a ještě složitějších stavů, jako je stárnutí, bude záviset na tom, jak zlepšíme naše způsoby, jak porozumět biologii, a také způsoby, jak ji upravit pomocí terapií.“
Další informace:
Sanju Sinha et al, DeepTarget předpovídá protirakovinné mechanismy působení malých molekul integrací léků a genetických screeningů, npj Přesná onkologie (2025). DOI: 10.1038/s41698-025-01111-4
Poskytuje
Sanford-Burnham Prebys
Citace: Výpočetní hloubkový ponor odhaluje skryté cíle proti rakovině a příležitosti pro nové využití (2025, 14. listopadu) získané 14. listopadu 2025 z https://medicalxpress.com/news/2025-11-deep-reveals-hidden-cancer-drug.html
Tento dokument podléhá autorským právům. Kromě jakéhokoli poctivého jednání za účelem soukromého studia nebo výzkumu nesmí být žádná část reprodukována bez písemného souhlasu. Obsah je poskytován pouze pro informační účely.




