Jediný imunitní protein může pomoci vysvětlit, proč se onemocnění ledvin a srdce často vyvíjejí společně
Rostoucí množství lidských, genetických a experimentálních důkazů naznačuje, že suPAR může nejen signalizovat riziko onemocnění, ale také aktivně přispívat k poškození orgánů, což vyvolává nové otázky o jeho roli jako klinického biomarkeru a terapeutického cíle.
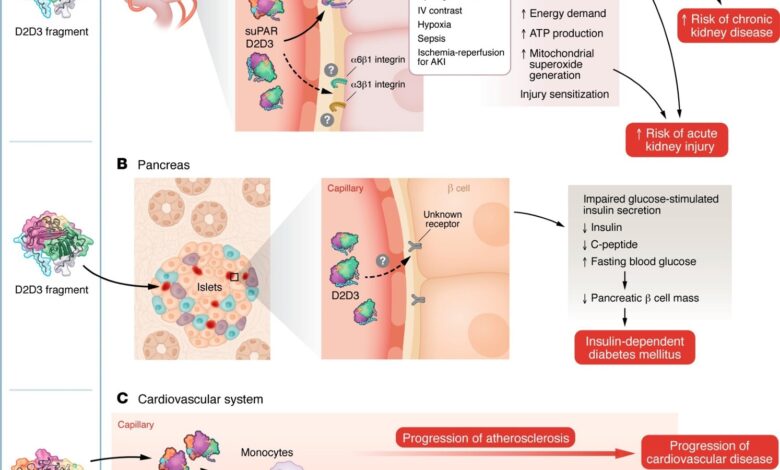
uPAR a jeho asociované proteiny indukují multiorgánové poškození. Dysregulace vrozené imunity způsobená různými fyziologickými problémy, jako je diabetes, hypertenze, virové a bakteriální infekce nebo kouření, vede ke zvýšeným hladinám suPAR a/nebo produkci proteinu D2D3. Modely ilustrují mechanismy, kterými tyto proteiny způsobují poškození ledvin (A), slinivka (Ba kardiovaskulární systém (C).
V nedávné studii publikované v Journal of Clinical Investigationvýzkumníci přezkoumali roli rozpustné formy (naštvaný) z uPAR a související proteiny při cukrovce a onemocněních srdce a ledvin.
Dysregulované nebo nadměrně aktivní vrozené imunitní reakce vedoucí k chronickým zánět jsou ústředními rysy poruch, jako je rakovina, cukrovka, onemocnění ledvin a kardiovaskulární onemocnění (CVD). Klíčovými přispěvateli k těmto procesům jsou interleukiny, chemokiny, interferon-γ, tumor nekrotizující faktor-α, aktivace zánětu, dysregulace komplementu a signalizace toll-like receptorů. uPAR je multiligandový, membránově vázaný receptor exprimovaný na imunitních a endoteliálních buňkách, kde reguluje imunitní aktivaci, buněčnou adhezi a remodelaci tkání.
uPAR podstupuje glykosylfosfatidylinositol (GPI)-kotevní štěpení a proteolytické zpracování za vzniku cirkulujících proteinů, včetně naštvaný a fragmenty D1 a D2D3. Na rozdíl od naštvanýD1 a D2D3 nejsou detekovatelné u zdravých jedinců, ale objevují se u pacientů s onemocněním ledvin a rakovinou. Navzdory strukturálním rozdílům se všechny cirkulující proteiny odvozené od uPAR podílejí na imunitní signalizaci a aktivaci buněk zprostředkované integrinem. Recenzovaná práce se zaměřila na podíl těchto proteinů na onemocnění ledvin, kardiovaskulární onemocnění a diabetes.
suPAR jako biomarker a mediátor u onemocnění ledvin
Za primární zdroj jsou považovány nezralé myeloidní buňky a neutrofily pocházející z kostní dřeně naštvaný při akutní aktivaci imunitního systému, takže cirkuluje naštvaný marker systémové vrozené imunitní aktivity spíše než poškození ledvin. Zvýšená naštvaný koncentrace byly trvale spojeny se zvýšeným rizikem onemocnění ledvin a rychlejší progresí poklesu renálních funkcí.
Jedna studie uvádí, že jedinci v nejvyšším kvartilu naštvaný hladiny zaznamenaly roční pokles odhadované glomerulární filtrace (eGFR) o 4,2 ml/min/1,73 m2a ti se zachovanou výchozí funkcí ledvin měli více než trojnásobně vyšší riziko progrese do stadia 3 chronického onemocnění ledvin (CKD). Napříč více kohortami, naštvaný byl jediný biomarker nezávisle spojené s poklesem funkce ledvin po úpravě podle věku, výchozí hodnoty eGFR, rasy, diabetu, hypertenze a proteinurie.
Genetické důkazy dále podporují roli pro naštvaný při onemocnění ledvin. Celogenomová asociační studie identifikovala missense variantu (rs4760) v genu PLAUR spojenou se zvýšenou cirkulací naštvaný úrovně. Mendelovské randomizační analýzy využívající tuto variantu poskytly důkaz konzistentní s kauzálním přínosem geneticky předpovězených naštvaný úrovně na CKD a aterosklerotické fenotypy, přičemž jsou uznávána metodologická omezení.
Přes tato zjištění, naštvaný měření zůstává v nefrologii kontroverzní. Samotná dysfunkce ledvin může přispět ke zvýšení naštvaný úrovně a naštvaný není vylučován primárně ledvinami, na rozdíl od kreatininu nebo cystatinu C. Navíc neexistují žádné testy schválené FDA pro naštvanýa současné enzymatické imunosorbentní testy mohou detekovat obojí naštvaný a D2D3, což komplikuje interpretaci. Než bude možné zvážit rutinní klinické použití, budou vyžadovány standardizované testy a přístupy složených biomarkerů.
suPAR, D2D3 a systémové účinky mimo CKD
Experimentální důkazy tomu nasvědčují naštvaný může ovlivnit metabolismus renálních tubulárních buněk. In vitro studie to ukázaly naštvaný zvyšuje produkci ATP, tvorbu mitochondriálního superoxidu a energetickou náročnost v proximálních tubulárních epiteliálních buňkách, potenciálně je senzibilizuje k poranění a pomáhá vysvětlit klinické souvislosti s akutním poškozením ledvin (AKI).
Klinické studie tyto asociace podporují. U pacientů podstupujících koronarografii, ti s nejvyšší naštvaný hladiny měly zvýšené riziko AKI a mortality. Podobně u AKI souvisejících se sepsí, naštvaný hladiny nad 12,7 ng/ml byly spojeny s vyšším rizikem renální substituční terapie a úmrtí, přičemž experimentální údaje naznačovaly imunitně zprostředkované mechanismy, jako je např. T buňka infiltrace.
Fragment uPAR D2D3 se účastní jak poškození ledvin, tak dysfunkce β-buněk pankreatu. U myší nadměrně exprimujících D2D3 se vyvinulo progresivní onemocnění ledvin a diabetes závislý na inzulínu bez dietních manipulací. In vitro a studie lidských ostrůvků ukázaly, že D2D3 inhiboval glukózou stimulovanou sekreci inzulínu. Údaje z pozorování dále naznačují, že diabetes je spojen se zvýšeným rizikem hematologických malignit a mortalitou, což naznačuje širší systémové důsledky signalizace související s uPAR.
suPAR v riziku a progresi kardiovaskulárních onemocnění
Mnohočetné kohortní studie prokázaly souvislosti mezi zvýšenými naštvaný koncentrace, subklinická ateroskleróza a budoucí kardiovaskulární příhody. Na rozdíl od reaktantů akutní fáze, jako je interleukin-6 nebo C-reaktivní protein, naštvaný hladiny zůstávají během akutního onemocnění stabilní a vykazují minimální cirkadiánní variace. naštvaný trvale překonává tradiční zánětlivé markery v predikci srdečního selhání, infarktu myokardu a aterosklerózy napříč různými populacemi.
Genetické studie tato pozorování potvrzují. Dvě varianty missense v PLAUR (rs2302524 a rs4760) byly spojeny s oběhem naštvaný a Mendelovské randomizační analýzy pomocí rs4760 naznačují, že vyšší naštvaný hladiny zvyšují riziko infarktu myokardu, onemocnění periferních tepen a onemocnění koronárních tepen. Replikace těchto zjištění napříč datovými soubory trans-předků podporuje, ale nedefinuje definitivně, kauzální roli.
Terapeutické důsledky a mezery ve znalostech
Celkově recenze vyzdvihuje vzájemně propojené mechanismy, kterými uPAR, naštvanýa D2D3 přispívají k poškození orgánů způsobené zánětem u ledvin, kardiovaskulárních a metabolických onemocnění. Zda terapeutické strategie zaměřené na snížení naštvanýbrzdící uPAR signalizace nebo odstranění patogenních fragmentů, jako je D2D3, se promítne do klinického přínosu zůstává nejisté, vzhledem k nedostatku intervenčních dat u lidí.
V současné době se žádná schválená terapie specificky nezaměřuje naštvanýale anti-naštvaný monoklonální protilátka (WAL0921) je hodnocena v klinických studiích fáze II, což odráží rostoucí zájem o translaci. Jako pochopení uPARPokud se signalizace rozšíří, mohou se tyto proteiny objevit jako cíle nejen u onemocnění ledvin, ale v rámci širšího spektra zánětlivých a kardiometabolických stavů.
Odkaz na deník:
- Reiser J, Hayek SS, Sever S (2026). Úloha suPAR a příbuzných proteinů u onemocnění ledvin, srdce a cukrovky. Journal of Clinical Investigation136(1), e197141. DOI: 10.1172/JCI197141, https://www.jci.org/articles/view/197141




