Mapa kontroly energie mozku nabízí plán pro terapie hubnutí příští generace
Hluboký ponor do mozkového příkazového centra hladu ukazuje, jak by dekódování jeho obvodů mohlo transformovat budoucnost ošetření hubnutí.
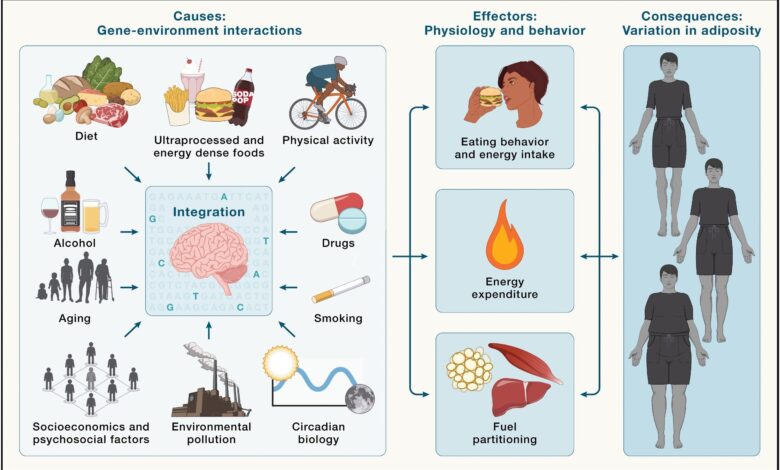
Integrace mozku environmentálních podnětů do regulace energetické bilance a adipozity – environmentální faktory (vlevo) jsou integrovány mozkem v kontextu genetického make -upu jednotlivce (ilustrované zvýrazněným SNP) a epigenetickým profilem. V reakci na to mozek reguluje behaviorální a fyziologické výstupy, jako je příjem energie, výdaje na energii a rozdělení paliva (uprostřed), které všechny ovlivňují rovnováhu energie, což nakonec formuje interindividuální změnu v adipozitě (vpravo).
V nedávné recenzi zveřejněné v časopise BuňkaSkupina autorů syntetizovala, jak centrální nervový systém (CNS) integruje neuroendokrinní signály, které řídí energetickou homeostázu a překládají tyto mechanismy do bezpečné a účinné farmakoterapie proti obizice.
Pozadí
Jak se systém přežití stal globální zdravotní krizí? Od 80. let 20. století vzrostla míra obezity a nyní postihla na celém světě asi jeden miliarda lidí, přičemž kardiovaskulární onemocnění řídila většinu úmrtí souvisejících s obezitou. Interakce genetiky a životního prostředí: Některá těla jsou připravena k přibírání na váze (hypotéza „drifty genu“), jiná odolávají a moderní potravinové narážky a stresory zesilují mezeru.
Patogeneze obezity zahrnují mechanismy „push“ (hyperfagie řízená mozkem) a „tažení“ (sekvestrace periferního paliva). Mezitím se mozkové obvody vyvinuly k obraně energetických obchodů, nikoli dnešních ultra zpracovaných stravy. Pochopení toho, jak je mozek, střeva, tuková tkáň a jaterní konverzace klíčem k vývoji bezpečných a účinných terapií anti-obezity. K mapování nervových obvodů a neuroplasticity závislé na aktivitě je zapotřebí dalšího výzkumu, které umožňují dlouhodobé, neaverzivní úbytek hmotnosti.
Neuroendokrinní mapa energetické homeostázy
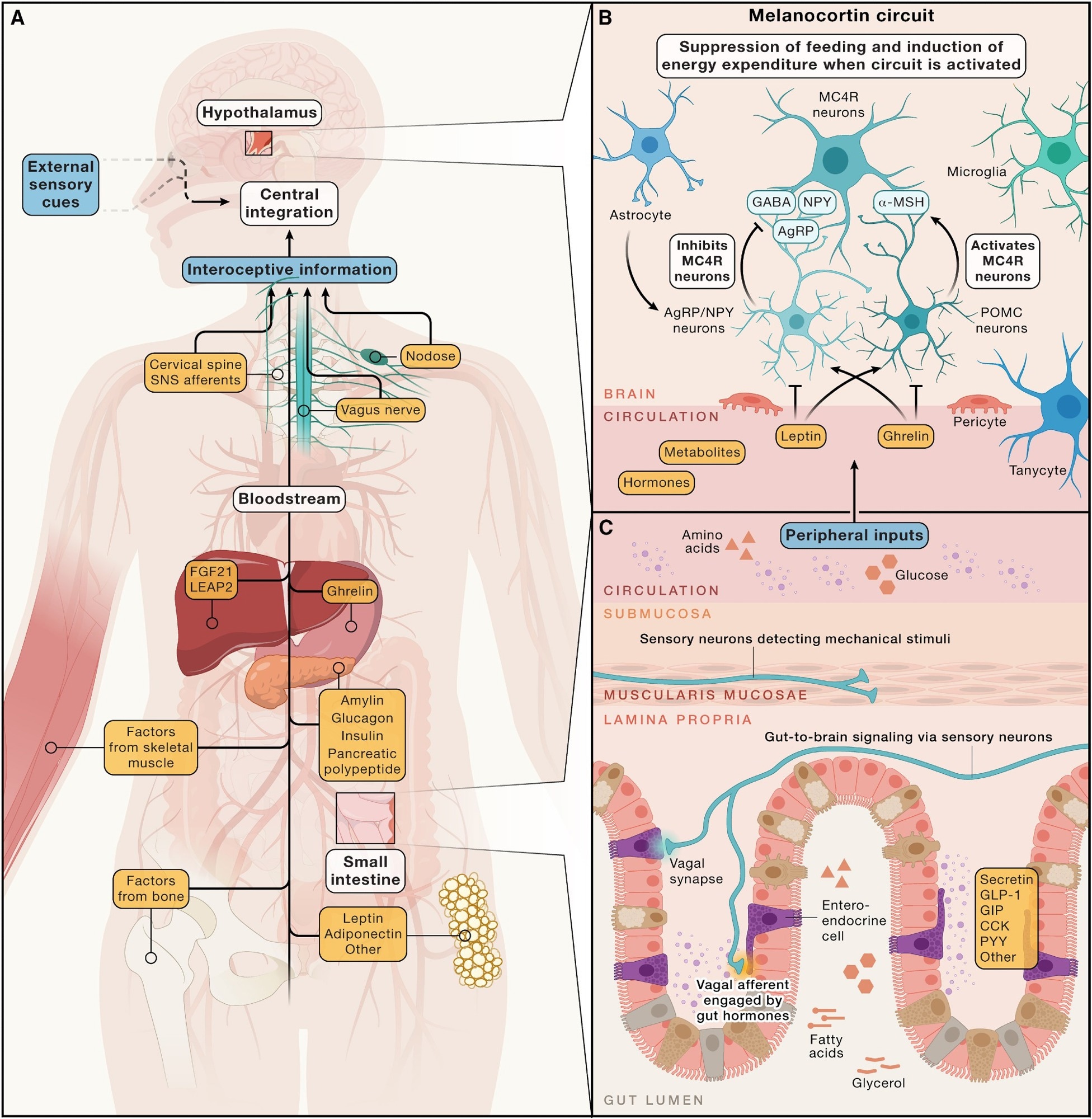
Energetická bilance mozkových arbitráží smícháním signálů pomalé adipozity s rychlými narážkami spojenými s jídlem. Stav tkáně tukové tkáně prostřednictvím leptinu, zatímco gastrointestinální (GI) trakt uvolňuje hormony jako Glukagon-jako peptid-1 (GLP-1), inzulinotropní polypeptid závislý na glukóze (GIP), cholecystokinin (CCK), peptid YY (pyy), sekretin a ghrelin (jediný orexigenní hormony v tomto seznamu) na žaludek na appite agotid (agrp) neurony. Tyto endokrinní signály doplňují vagální a páteřní aferenty, které cítí distanzi střev a živiny, což poskytuje rychlou zpětnou vazbu CNS.
Společně endokrinní a nervové vstupy koordinují trávení, sytost a metabolickou homeostázu. Játra přidává svůj hlas, fibroblastový růstový faktor 21 (FGF21), inzulínový růstový faktor 1 (IGF-1) a jaterní antimikrobiální peptid 2 (LEAP2), zatímco malé metabolity a žlučové kyseliny obcházejí zprávu.
Hypothalamické obvody: Nastavení energetického rozpočtu
Obloukové jádro (ARC), sousedící s mediánskou eminence (obezřetný orgán (CVO)), má privilegovaný přístup k cirkulujícím hormony a metabolitům. ARC neurons express receptors for leptin, ghrelin, and insulin and receive inputs from the paraventricular hypothalamus (PVH), ventromedial hypothalamus (VMH), and dorsomedial hypothalamus (DMH), and extrahypothalamic hubs such as the bed nucleus of the stria terminalis (BNST) and nucleus of the solitary tract (NTS).
Hunger-promoting AgRP neurons release γ-aminobutyric acid (GABA), neuropeptide Y (NPY), and AgRP to inhibit satiety circuits, while pro-opiomelanocortin (POMC) neurons release α-melanocyte-stimulating hormone (α-MSH) to activate melanocortin 4 receptor (MC4R) neurons and curb intake. Synaptická plasticita v těchto obvodech (např. Reorganizace vstupů závislá na leptinu) se přizpůsobuje energetickým stavem. Tyto výstupy ARC projektují široce a umožňují hypotalamickým sítím nastavit chuť k jídlu a výdaje.
Hindbrain & Vagal Control: Sitety bez nemoci
Dorsální vagální komplex (DVC) integruje viscerální signály pro ukončení jídla. V NTS, neurony receptoru kalcitoninu (CALCR), včetně podmnožiny peptidu uvolňujícího prolaktin (PRLH), potlačují krmení bez averze a mohou omezit hlad poháněný AGRP polysynaptickými dráhami.
Naproti tomu obvody oblasti Postrema (AP) mohou spárovat potlačení chuti k jídlu s malátností: Faktor rozlišení růstu 15 (GDF15) působí prostřednictvím přes gliová buňka Neurotrofní faktor (GDNF) receptor alfa podobný (GFRAL) neurony, které aktivují parabrachiální buňky peptidu (CGRP), které aktivují parabrachiální buňky peptidu (CGRP).
Receptor peptid-1 receptoru GLP-1R) specifického pro region: GLP-1R Akce v averzi AP řídí averzi GLP-1R v NTS podporuje sytost a naznačuje, proč některé léky se cítí hladolnější než jiné.
Hormonální, metabolické a nervové vstupy do mozkových obvodů regulujících energetickou homeostázu – (a) Zjednodušený přehled periferních signálů vyplývajících z více orgánových systémů spolu se smyslovými narážkami z vnějšího prostředí. Tyto signály jsou integrovány centrálním nervovým systémem pro regulaci příjmu energie a výdajů na energii a v průběhu času udržují stabilní adipozitu. Tato regulace zahrnuje jak dlouhodobé signály skladování energie, jako je leptin, tak krátkodobé signály související s okamžitým příjmem energie, jako jsou gastrointestinální hormony a živiny. (B) Obloukové jádro hypothalamu obsahuje obvod melanokortinu, který vysoce reaguje na odchylky v cirkulujících hormonech (např. Nurs z gastrointestinálního traktu) a tukové tkáně a metabolitů. Ústředním bodem tohoto obvodu jsou AGRP neurony podporující hlad a neurony podporující sytost. Tyto neuronální populace modulují energetickou rovnováhu prostřednictvím inhibičních a excitačních vstupů do dolních neuronů exprimujících MC4R. C) Mnoho periferních vstupů ovlivňujících mozkové obvody, které regulují energetickou bilanci, pochází ve střevě. Enteroendokrinní buňky uvolňují hormony, jako je sekretin, GLP-1, GIP, CCK a další, do oběhu v reakci na různé podněty, jako je přítomnost luminálních živin. Kromě toho vagální aferenty přenášejí mechanické a chemické informace – jako jsou střevní distenze a obsah živin – od gastrointestinálního traktu po mozek.
Motivace a odměna: Proč chutná jídla vyhrají
Mezokortikolimbické dráhy, ventrální tegmentová oblast (VTA) dopaminové projekce do jádra accumbens (NAC) a prefrontální kůry, přiřazují pobídkové významy potravinářským podnětům. Rozhraní laterálního hypotalamu (LH) s těmito obvody odměňování prostřednictvím melaninového koncentrujícího hormonu (MCH) a orexinu neuronů, které se promítají na VTA a NAC a zaujatost hledající chutné potraviny. Vzhledem k tomu, že homeostatické a hedonické systémy blokovaly, musí efektivní terapie tlumit pohon k jídlu bez zploštění každodenní motivace. Signalizace střeva na mozek prostřednictvím vagu může aktivovat dopaminové neurony po snímání cukru a pomoci vysvětlit, proč se ultra zpracovaná jídla cítí přesvědčivá i bez silných vkusů.
Od obvodů po léky: Co funguje nyní
Dřívější léky fungovaly hlavně prostřednictvím monoaminů (dopamin, norepinefrin, serotonin), jako v phentermin-topiramátu nebo bupropionu-nealtrexonu, což přineslo přibližně 8% -10% ztrátu u kardiovaskulárních, GI a psychiatrických kompromisů. Peptidové inženýrství změnilo hru: reverzibilní vazebná albumin prodloužený poločas inkretinu, což umožňuje terapie GLP-1; Liraglutid způsobil ztrátu 56 týdnů s korigovanou placebem 56 týdnů u lidí s obezitou bez diabetu.
Společné zapojení inzulinotropního polypeptidového receptoru závislého na glukóze (GIPR) může tupé averze spojené s GLP-1R při zachování potlačení příjmu, jeden věrohodný důvod duální inkretiny dosahuje větší úbytek hmotnosti. Agonisté amylinové receptor (Amyr), kteří působí prostřednictvím komplexů proteinu modifikujících aktivity modifikující CalCR-receptor (RAMP) v AP a ARC, také potlačují příjem a mohou tak učinit s méně averzivními signály. Pozoruhodné je, že jednomolekula GLP-1R/Amyr Coagonistka amycretin vedla 24% úbytek hmotnosti ve studii fáze 1/2.
Mezery v znalostech s sázkami v reálném světě
Mezi klíčové neznámé patří to, které populace neuronů udržují neaverzivní sytost, jak strava a stres přetvářejí synapse v hypotalamických, hindbránových a odměňovacích sítích a jak „bezpečně převádět“ maladaptivní obvody. Odpověď na tyto otázky by zdokonalovala terapii specifickou pro pacienta (výběr inkretinové páteře, doplňky amylinového receptoru), snížili přerušení a rozšířili kardiometabolické výhody pro rodiny a zdravotnické systémy pro mnoho pacientů.
Závěry
Abych to shrnul, mozek je příkazovým centrem homeostázy energie. Integrací endokrinních signálů z tukové tkáně, traktu GI, břišní a játra s rychlým nervovým vstupem, centrálním obvodem, od obloukových melanokortinových cest po DVC a mezokortikolimbické sítě, nastavené chuti, výdaje a odměňování.
Peptidové farmakoterapie, které se zaměřují na dráhy GLP-1R, GIPR a amylinu, již přinášejí smysluplné hubnutí. Budoucí úspěch bude záviset na neuroplasticitě závislé na aktivitě a na navrhování kombinací, které maximalizují sytost, minimalizují averzi a chrání dlouhodobé kardiometabolické zdraví pro lidi všude.
Reference časopisu:
- Johansen, VBI, Petersen, J., Lund, J., Mathiesen, CV, Fenselau, H., & Clemmensen, C. (2025). Kontrola mozku energetické homeostázy: Důsledky pro farmakoterapii anti-obezity. Buňka188 (16), 4178–4212. Doi: 10.1016/j.cell.2025.06.010 https://www.cell.com/cell/fulltext/s0092-8674(25)00677-4