Parkinsonova choroba může pramenit spíše z hladovění železem než z přetížení železem
Nové důkazy naznačují, že zachycení železa v nepoužitelných formách může vyhladovět zranitelné neurony, což zpochybňuje desetiletí přemýšlení o toxicitě železa u Parkinsonovy choroby a otevírá nové terapeutické otázky.
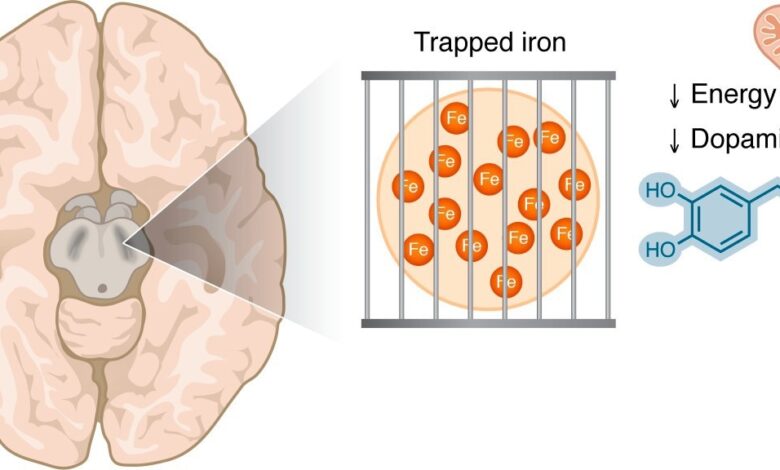
Akumulace železa v substantia nigra je viditelná pomocí technik MRI u pacientů s PD. Toto železo může být v zachycené formě, takže je nedostupné pro biologické procesy závislé na železe, které jsou kritické v dopaminergních buňkách, včetně mitochondriálního dýchání a syntézy dopaminu.
V nedávném pohledu zveřejněném v Journal of Clinical Investigationvýzkumníci diskutovali o důkazech, které zpochybňují dlouhotrvající vědeckou víru, že se běžně předpokládá, že Parkinsonova nemoc je způsobena přetížením toxickým železem v mozku. Místo toho tvrdili, že onemocnění může zahrnovat funkční nedostatek železa, při kterém je biologicky využitelné železo nízké navzdory vysokému celkovému obsahu železa a může koexistovat s regionálně zvýšenými signály železa. Obnovení dostupnosti železa, spíše než jeho odstranění, by mohlo představovat možnou cestu léčby.
Po desetiletí byla abnormální akumulace železa spojována s Parkinsonovou chorobou, zejména v substantia nigra, což je oblast mozku nejvíce postižená u pacientů s tímto onemocněním. Tato asociace vedla k dominantní hypotéze, že přebytek železa pohání neurodegeneraci prostřednictvím oxidačního stresu a drah buněčné smrti závislé na železe, jako je ferroptóza, ačkoli kauzální role ferroptózy u Parkinsonovy choroby zůstává diskutována.
Nedávné klinické studie naznačují, že chelátování železa s látkou penetrující do mozku deferipronem může zhoršit symptomy, zejména u pacientů, kteří dosud nezahájili dopaminergní terapii. Tyto neočekávané nálezy si vynutily přehodnocení role železa u Parkinsonovy choroby a otevřely dveře alternativnímu vysvětlení, funkčnímu nedostatku železa. V takových případech jsou celkové hladiny železa normální nebo možná zvýšené, dokonce i jako biologicky dostupné železnaté železo (Fe2+), která je nezbytná pro buněčné procesy, je nedostatečná.
Od náhrady dopaminu k biologii železa
Moderní léčba Parkinsonovy choroby začala objevem, že levodopa (L-DOPA) může obnovit motorické funkce kompenzací ztráty dopaminu v bazálních gangliích. Tato strategie byla následně podpořena důkazy prokazujícími sníženou aktivitu tyrosinhydroxylázy (TH), enzym závislý na železe zodpovědný za zahájení syntézy dopaminu. Časné biochemické studie prokázaly, že železo silně stimuluje aktivitu TH.
Tyto poznatky podnítily rané klinické experimenty se suplementací železa. Zprávy publikované během 80. let minulého století popisovaly podstatné zlepšení symptomů u pacientů s Parkinsonovou nemocí, kteří dostávali léčbu železem. Někteří byli schopni omezit nebo vysadit dopaminergní léky. Ačkoli tyto studie postrádaly moderní design zkoušek, vyvolaly možnost, že nedostatek železa, spíše než nadbytek, by mohl omezit produkci dopaminu u pacientů s tímto onemocněním.
Hypotéza toxicity železa
Navzdory časným náznakům, že železo by mohlo být prospěšné, došlo k výraznému posunu směrem k hypotéze přetížení železem, protože zobrazovací a histologické studie odhalily zvýšené signály železa v substantia nigra u Parkinsonovy choroby. Tato zjištění v kombinaci s rostoucím zájmem o oxidační stres a feroptózu posílily přesvědčení, že přebytek železa je toxický a měl by být odstraněn.
Nedostatečný přínos a potenciální poškození pozorované ve studiích chelace železa však tento model přímo zpochybňují. Pokud by přetížení železem skutečně způsobilo Parkinsonovu nemoc, odstranění železa by mělo mít lepší výsledky. Namísto toho zhoršující se symptomy naznačují, že odstranění železa může připravit již tak zranitelné neurony o železo, které potřebují k přežití a funkci, zejména v časnějších stádiích onemocnění.
Zjevné přetížení železem může být zavádějící
Klíčovým poznatkem této perspektivy je, že ne všechno železo je biologicky ekvivalentní. Železné železo (Fe3+), který je relativně inertní, je snadněji detekován MRI a histologické techniky, protože je uložen v hustých formách, jako je feritin a neuromelanin. Naproti tomu Fe2+ je aktivní forma potřebná pro enzymatické reakce, syntézu dopaminu a mitochondriální dýchání.
MRI nedokáže rozlišit mezi Fe3+ a Fe2+ani nemůže určit, které typy buněk nebo subcelulární kompartmenty obsahují železo. V důsledku toho mohou zvýšené signály MRI železa odrážet sekvestraci nevyužitelného Fe3+ spíše než přebytek funkčního železa. Podobné vzorce se vyskytují během chronických zánětkde je železo sekvestrováno do zásobních forem, což vede k hladovění buněčného železa navzdory zvýšeným hladinám železa v tkáních.
Další mechanismy mohou tento problém u Parkinsonovy choroby zhoršit, včetně lysozomální dysfunkce, která brání uvolňování železa do cytoplazmy a sekvestraci železa uvnitř gliových buněk spíše než dopaminergní neurony. Společně by tyto procesy mohly vytvořit iluzi přetížení železem, zatímco samotné neurony zažívají nedostatek železa.
Podpora pro nízkou biologickou dostupnost železa
Několik linií důkazů posiluje hypotézu funkčního nedostatku železa. Poruchy, jako je manganismus, připomínají Parkinsonovu chorobu a narušují manipulaci se železem, čímž snižují aktivitu enzymů závislých na železe, jako je TH a mitochondriální akonitáza. Podobně genetické podmínky seskupené pod BIA vykazují hromadění železa, zhoršené využití železa a dopaminergní dysfunkci.
Experimentální studie poskytují přímější podporu. Delece transferinového receptoru v myších dopaminergních neuronech způsobuje nedostatek železa, ztrátu neuronů a motorické symptomy podobné Parkinsonovi. Epidemiologická data také spojují anémii a nedávné dárcovství krve se zvýšeným rizikem Parkinsonovy choroby, ačkoli tyto souvislosti jsou pozorovací a nemohou prokázat kauzalitu.
Důsledky pro budoucí terapii
Celkově vzato důkazy zpochybňují myšlenku, že přetížení železem je primární hnací silou Parkinsonovy choroby. Místo toho je mnoho nálezů lépe vysvětleno modelem funkčního nedostatku železa, kde je železo přítomno, ale biologicky nedostupné. Tento rámec vysvětluje, proč chelace železa může zhoršovat symptomy a proč obnovení biologické dostupnosti železa, spíše než bezohledné odstranění železa, může vyžadovat další zkoumání, při zohlednění stadia onemocnění a předchozí dopaminergní léčby.
Odkaz na deník:
- Peikon, I., Andrews, NC (2026). Není to ironie? Funkční nedostatek železa v jádru patobiologie Parkinsonovy choroby. Journal of Clinical Investigation. DOI: 10.1172/JCI202244, https://www.jci.org/articles/view/202244




