Bakterie tuberkulózy deaktivuje klíčový imunitní senzor, aby se vyhnul obraně hostitele, odhaluje studie
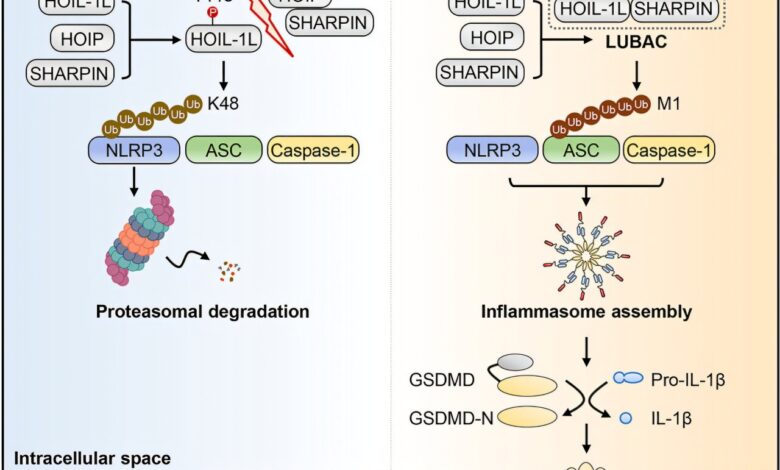
MTB PKNG unáší komplex sestavy sestavy řetězce hostitele lineárního ubikvitinu, aby se vyhýbala cytosolickému imunitnímu dohledu zprostředkovanému zánětlivým nlrp3. Kredit: Skupina Liu Cuihua
Výzkumný tým odhalil nový mechanismus, který umožňuje mycobacterium tuberculosis (MTB), bakterii, která způsobuje tuberkulózu (TB), vyhnout se imunitní obraně hostitele.
Studie zveřejněná v Buněčné zprávyUkazuje, jak MTB unáší lineární ubikvitinový stroj hostitele, aby řídil degradaci nlrp3 zánětlivého, čímž působil proti intracelulárnímu imunitnímu dohledu hostitele.
MTB nadále představuje hrozbu pro pacienty v důsledku vzniku a šíření antimikrobiální rezistence. Hostitel Imunitní buňky mají cytosolické senzory, které detekují napadající patogeny a iniciují protiinfekční reakce. Jak patogeny, jako je MTB, však podkopává intracelulární dohled hostitele, který způsobuje přetrvávající infekci, není však zcela objasněno.
V této studii vědci, vedeni prof. Liu Cuihua z Institutu mikrobiologie Čínské akademie věd, zjistili, že PKNG, proteinová kináza vylučovaná MTB (Lubac) narušuje Imunitní odpovědi NLRP3.
Mechanicky PKNG fosforyluje podjednotku HOIL-1L LUBAC, což zabraňuje účasti na tvorbě LUBAC HOIL-1L. Toto narušení zhoršuje LUBAC-závislou lineární ubikvitinaci zánětlivého adaptéru ASC, což nakonec inhibuje sestavu zánětlivých zánětlivých NLRP3.
Navíc fosforylace zprostředkovaná PKNG současně aktivuje vnitřní aktivitu E3 ubikvitin ligázy HOIL-1L, což umožňuje HOIL-1L zprostředkovat ubikvitinaci spojenou K48 a následnou degradaci NLRP3.
Abych to shrnul, prostřednictvím tohoto mechanismu s dvojitou regulací, který dosahuje efektu „jeden kamenný-dva-birds“, jak je uvedeno výše, může PKNGG podpořit únik MTB z NLRP3-zprostředkovaného cytoplazmatického imunitního dohledu, a tím dále usnadňuje intracelulární přežití a infekci patogenu.
Tato studie ukazuje, že MTB využívá fosforylační dynamiku hostitelského lineárního ubikvitinového stroje prostřednictvím interakce PKNG/HOIL-1L. Tato interakce tvoří mezidruhovou enzymatickou kaskádu, která řídí degradaci senzoru zánětlivých, což umožňuje MTB působit proti NLRP3-závislému imunitnímu dohledu.
Tato zjištění také poskytují potenciální strategii pro terapii anti-TB a optimalizaci vakcíny proti Bacille Calmethe-Guérin (BCG) zaměřením na rozhraní PKNG/HOIL-1L.
Více informací:
Yang Yu a kol., Patogenní fosforylace lineárního ubikvitinového aparátu způsobuje degradaci senzoru zánětlivého, degradace senzoru zánětlivých Buněčné zprávy (2025). Doi: 10.1016/j.celrep.2025.116286
Poskytnuto
Čínská akademie věd
Citace: Tuberculosis Bakterie deaktivuje klíčový imunitní senzor, aby se vyhnul obraně hostitele, odhaluje studie (2025, 19. září) získaná 20. září 2025 z https://medicalxpress.com/news/2025-09-tuberculosis-tacterium–Kye-imune.html
Tento dokument podléhá autorským právům. Kromě jakéhokoli spravedlivého jednání za účelem soukromého studia nebo výzkumu nemůže být žádná část bez písemného povolení reprodukována. Obsah je poskytován pouze pro informační účely.




