Drobné 3D tiskové přeplňovací inženýrství s bezprecedentní přesností

Zařízení je dostatečně kompaktní, aby spočívalo na prstu a je kompatibilní s současnou technologií tkáňového inženýrství.
Nově vyvinuté zařízení 3D potištěné nabízí vědcům schopnost budovat modely lidských tkání s mnohem větší přesností a složitostí. Nástroj vytvořený interdisciplinárním týmem na University of Washington a UW Medicine je navržen tak, aby se snadno integroval do stávajících laboratorních metod.
Nedávný pokrok ve 3D tkáňovém inženýrství již zlepšil rychlost a přesnost stavebních systémů, které poskytují biomedicínské vědce silné nové způsoby, jak navrhnout a testovat ošetření pro širokou škálu nemocí. Ústředním cílem pole je znovu vytvořit laboratorní prostředí, která napodobují přirozené podmínky, které buňky zažívají uvnitř těla.
Jedna běžná metoda zahrnuje pozastavení buněk v gelu umístěném mezi dvěma volně stojícími sloupky. Toto nastavení bylo použito k pěstování tkání, jako je srdce, plíce, kůže a svaly. Přestože je přístup účinný při umožnění buňkám fungovat životem, přístup má omezení: je obtížné prozkoumat, jak interaguje více typů tkání. Dosažení jemnější kontroly nad složením a uspořádáním buněk by mohlo umožnit modelovat komplexní podmínky, včetně neuromuskulárních poruch.
Stomp umožňuje vzorované tkáňové prostředí
Příspěvek publikovaný v Pokročilá věda Podrobnosti o tom, jak nová platforma umožňuje vědcům zkoumat, jak buňky reagují na mechanické a fyzické narážky, přičemž vytvářejí odlišné oblasti v zavěšené tkáni. 3D tiskové zařízení je známé jako Stomp (suspendované tkáňové otevřené mikrofluidní vzorce).
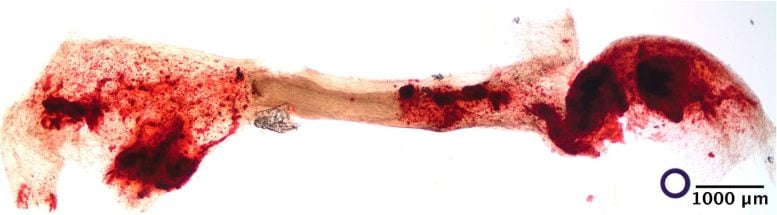
Ashleigh Theberge, profesor chemie UW a Nate Sniadecki, profesor strojního inženýrství a prozatímní kodirector UW Medicine Institute for Smenové buňky a regenerativní medicínu, vedli vědecký tým. Skupina ukázala, že jejich zařízení může znovu vytvořit biologická rozhraní, jako je kosti a vaz nebo fibrotická a zdravá srdeční tkáň.
Prvními autory příspěvku byli Amanda Haack, studentka lékařského vědeckého programu School of Medicine a postdoktorandská kolega v Laboratoři Theberge, a Lauren Brown, Ph.D. Student v chemii. Členové fakulty UW Cole DeForest, profesor chemického inženýrství a bioinženýrství, a Tracy Popowics, profesor ústní biologie na School of Dentistry, jsou spoluautory.
Lití tkání s mikrofluidní přesností
Stomp staví na technice tkáňového inženýrství známého jako casting, kterou vědci popisují jednoduchou analogií výroby Jell-O ve formě. V laboratorní praxi je „gel“ směsí živých a syntetických materiálů, umístěných do podpůrného rámu s pipetou, spíše než vylévanou. Stomp zaujme tento přístup dále pomocí kapilární akce-podobné způsobu, jakým voda stoupá ve slámě-umožnit vědcům přesně umístit různé typy buněk ve zvolených vzorcích, podobně jako uspořádání ovocných kusů rovnoměrně do Jell-O.
Pro vyhodnocení jeho potenciálu tým testoval Stomp ve dvou experimentech: jeden zkoumal kontraktilní chování inženýrské srdeční tkáně v nemocných i zdravých stavech, zatímco druhý obnovuje vaz, který zajišťuje zub v kostní soketu.
Samotné zařízení má pouze velikost prstu. Připojuje se k dvoubodové platformě původně navržené laboratoří Sniadecki pro měření kontraktilních sil srdečních buněk. V této malé struktuře leží otevřený mikrofluidní kanál vybavený geometrickými rysy, které řídí jak rozestupy, tak uspořádání typů buněk, což umožňuje vytvoření odlišných oblastí v zavěšené tkáni – to vše bez vyžadování dalších nástrojů nebo přidané složitosti.
Konstrukční funkce zlepšují všestrannost tkáně
Technologie hydrogelu z DeForest Research Group se potlačila s dalším designovým prvkem: rozložitelné stěny. Tkáňoví inženýři mohou rozbít strany zařízení a nechat tkáně neporušené.
„Normálně, když vložíte buňky do 3D gelu,“ řekl Sniadecki, „použijí své vlastní kontraktilní síly k tomu, aby všechno spojily dohromady – což způsobí, že se tkáň zmenšuje od stěn formy. Ale ne každá buňka je super silná a ne každý biomateriál se tak může převzít.
Theberge je nadšený tím, jak ostatní týmy budou používat Stomp.
„Tato metoda otevírá nové možnosti pro výzkum tkáňového inženýrství a signalizace buněk,“ řekla. „Bylo to skutečné týmové úsilí více skupin pracujících napříč disciplínami.“
Reference: „Pozastavená tkáň Otevřená mikrofluidní vzorce (Stomp)“ od Amanda J. Hack, Lauren G. Brown, Alex J. Goldstein, Priti Mulimani, Jean Berthier, jako R. Viswanathan, Copyeva, Jamison M. Whitten, Serena H. Nguyen, Thoome A. P. Leahy, Thoome. C. Tokihiro, Ross C. Brethah Wu, Stephen J. Tapscott, Cole A. DeForest, Traccy E. Nathan J. Sniadecki a Ashleigh B. Theberge, 29. dubna 2025, Pokročilá věda.
Doi: 10.1002/advs.202501148
The Národní zdravotní ústavy (NIH) podporoval výzkum prostřednictvím R35GM128648, R35GM138036, R01HL149734, R03DE029827, T32CA080416, F30HL158030, R90DE023059, 5TL1TR002318-08 a A A A A A A A A A A A A A A A A A A A A A A A A A A A A A A A A A. R35GM128648. Tato práce byla také částečně podporována UW, Friends of FSH Research, Chris Carrino Foundation for FSHD a stipendijní fondy od senátora Paula D. Wellstona Muscular Dystrophy Specialized Research Center – Seattle (Niams P50AR065139) a dar ionis farmaceuticals.
Nikdy nezmeškáte průlom: Připojte se k zpravodaji Scitechdaily.