Lenacapavir: Po schválení FDA se HIV předběžná profylaxe injektovatelná blíže ke schválení EU
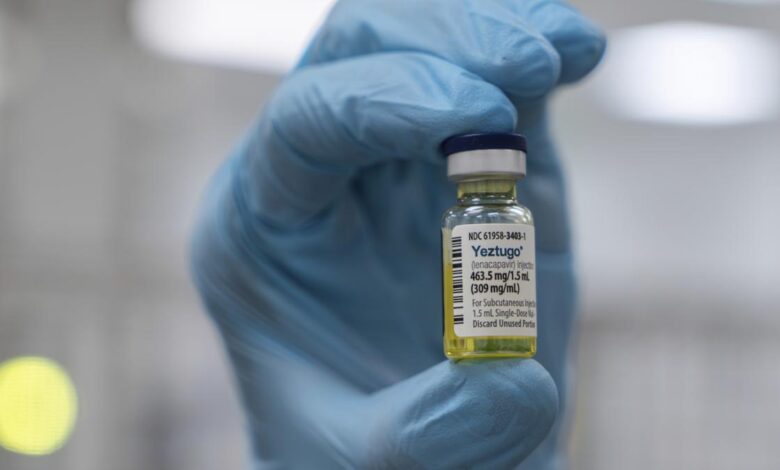
25. července poradní výbor Evropské léčivé agentury (EMA) doporučeno Lenacapavir Gilead Sciences, dvakrát roční injekce, za prevenci infekce HIV u dospělých a dospívajících. Jakékoli doporučení poradního výboru EMA musí být formálně schváleno Evropskou komisí, která se očekává koncem tohoto roku. Doporučení poradního výboru EMA přichází asi měsíc poté, co americká FDA 18. června 2025 schválila injekční inhibitor kapsidu HIV-1 jako profylaxi před expozicí (PREP).
Světová zdravotnická organizace přivítal souhlas FDA 19. června a vydané pokynyS pro použití lenacapaviru pro prevenci HIV 14. července. „Nabízení další volby profylaxe (PREP) má potenciál zvýšit absorpci a efektivní využití přípravy a celkově prevence HIV, protože umožňuje lidem zvolit metodu, kterou preferují,“ uvádí pokyny. Studie také ukázaly, že lenacapavir může dosáhnout významného potlačení viru, a to i v případech, kdy selhaly jiné léky.
Lenacapavir schválený FDA je založen na výsledcích roku 2024 z pokusů s účelem 1 a účel 2, které prokázaly bezpečnost a účinnost profylaxe před expozicí v injekci napříč různými populacemi a nastaveními. Účelem 1 byla fáze 3, dvojitě zaslepená, randomizovaná studie pro vyhodnocení bezpečnosti a účinnosti dvakrát ročně, subkutánní lenacapavir pro profylaxi před expozicí (PREP) a byla testována na 5 338 cisgenderových ženách a dospívajících dívek ve věku 16–25 let v Jihoafrickém republice a na třech místech v Ugandě. Injektovatelný byl porovnán s aktivním kontrolním ramenem, které kdysi obdrželo profylaxis léčiva Truvada jednou denně (emtricitabin-tenofovir disoproxil fumarát; F/TDF). Mezi 2 134 účastníky ve skupině Lenacapavir byly mezi 2 134 účastníky HIV infekce, zatímco aktivní kontrolní skupina měla 39 infekcí mezi 2 136 účastníky.
V Účel 2 fáze 3 pokus Zahrnující 3 265 účastníků do modifikované analýzy záměru na léčbu byli dva účastníci infikováni HIV v rameni, které dostaly injekční, zatímco devět účastníků, kteří obdrželi aktivní kontrolní přípravu perorální léčivo Truvada (emtricitabin-tenofovir disoproxil fumarát; F/TDF). Incidence HIV na pozadí v populaci prověřené (4 634 účastníků) byl 2,37 na 100 osob. Soud byl proveden v cisgenderových mužch, transgenderových a nebinárních jednotlivcích na 88 místech v Argentině, Brazílii, Mexiku, Peru, Jižní Africe, Thajsku a USA
Ve srovnání s obecným přípravným lékem Truvada, který je extrémně levný a široce dostupný, stojí lenacapavir 28 000 $ za dvě injekce. Proč by lidé někdy raději používali lenacapavir zvažování nákladů? „Ústní příprava bude účinná pouze tehdy, pokud dojde ke 100% dodržování. Ústní lék nebude fungovat, i když bude chybět na den, protože úroveň drog bude jen 24 hodin,“ říká Dr. N. Kumarasamy, šéf a ředitel VHS-infekční lékařské středisko, dobrovolné zdravotnické služby, Chennai.
„Lidé, kteří mají nejvyšší riziko, jako jsou sexuální pracovníci a homosexuální muži, musí drogu užívat každý den. Užívání tabletu každý den, a to i pro zesnulého pacienta, je tak obtížné. Má tendenci minout dávku, a proto není dodržování nikdy 100%,“ říká. „Dokonce i v případě přípravy na vyžádání, kde lidé, kteří se chtějí dopřát nechráněnému pohlaví, musí užívat ústní léčivo dva dny předtím, pak během období rizikového chování a pokračovat další dva dny po skončení rizikového chování, adherence nikdy nepřesahuje 85–90%. Prep bude fungovat pouze v případě, že dodržování bude 100%.“
Podle Dr. Kumarasamyho, přestože je perorální tableta levná a snadno přijímána, je dodržování menší než ideální, důvod, proč se lidé pohybují směrem k dlouhodobě působícím injekčnímu, které zabraňují infekci HIV měsíce po injekci. Cabotegravir, který byl vyvinut jako profylaxe před expozicí (PREP), podstoupil pokusy v mnoha zemích a byl schválen pro použití. Cabotegravir, který je podáván intramuskulárně každé dva měsíce, byl nalezen lepší ve srovnání s každý den orální přípravné tablety a začal být implementován v určitých částech světa, říká Dr. Kumarasamy.
„Vzhledem k tomu, že CaboteGravir musí být podáván každé dva měsíce, lidé mají tendenci zapomenout. Nový lék Lanacapivir byl shledán účinným po dobu šesti měsíců v pokusech. Injekční injekční byla vyvinuta v roce 2021 jako léčba u lidí, kteří již na jiné drogy nereagují, protože vyvinuli rezistenci,“ říká.
Protože bylo zjištěno, že lenacapavir je dlouhodobě, byl repeponován jako profylaxe před expozicí podávaná subkutánně. “Lenacapavir is a robust molecule and is the best solution in the absence of vaccines. Even if there is going to be an HIV vaccine one day, I’m sure people will have to take the vaccine every year or something. Like a flu shot, you know if at all they are going to develop a vaccine, people may have to take it every year or every six months as a booster dose. It may not be like a one dose that is effective for years,” Dr. Kumarasamy říká. „Při absenci vakcíny proti HIV si myslím, že profylaxi před expozicí každých šest měsíců lze považovat za vakcínu.“
Gilead vyvíjí stejnou molekulu, která se podává jednou ročně namísto každých šest měsíců. Už na tom pracují. Nebude to však subkutánní forma, ale jako intramuskulární injekce, říká.
Licenční dohody
2. října 2024, Gilead Sciences podepsal Nevyhnutelné, bezplatné dobrovolné licenční dohody se šesti farmaceutickými výrobci k výrobě a prodeji generického lenacapaviru. Ze šesti generických výrobců jsou čtyři v Indii. Kromě dohody o podpisu na licenci generických výrobců, kteří budou injekční, Gilead Sciences rovněž uvedl, že „by podpořil levný přístup k léku ve vysokých issistenčních zemích, bez zisku, dokud generičtí výrobci nebudou schopni plně podporovat poptávku“. Tyto země jsou: Botswana, Eswatini, Etiopie, Keňa, Lesotho, Malawi, Mozambik, Namibie, Nigérie, Filipíny, Rwanda, Jižní Afrika, Tanzanie, Thajsko, Uganda, Vietnam, Zambabwe.
Společnost získala licenci Dr. Reddy’s Laboratories Limited, Emcure, Hetero a Mylan, dceřinou společnost Viatris, na výrobu lenacapaviru v Indii. Společnosti budou mít povoleno dodávat do 120 zemí. Podle tiskové zprávyDohody zahrnují nejen lenacapavir pro prevenci HIV, ale také pro léčbu HIV u dospělých s těžce léčbou (HTE) s více léčivým rezistentním HIV.
Podle Dr. Kumarasamy One společnost již začala rozvíjet lék a Lenacapavir může být k dispozici příští rok, jakmile indický regulační orgán jej schválí na základě výsledků bezpečnostní studie provedené v Indii. Podle jeho odhadu bude obecná forma lenacapaviru stát asi 100 USD za dávku.
Publikováno – 27. července 2025 03:10




