Poškození mrtvice se obrátilo, když se kmenové buňky znovu dozvěděli mozek
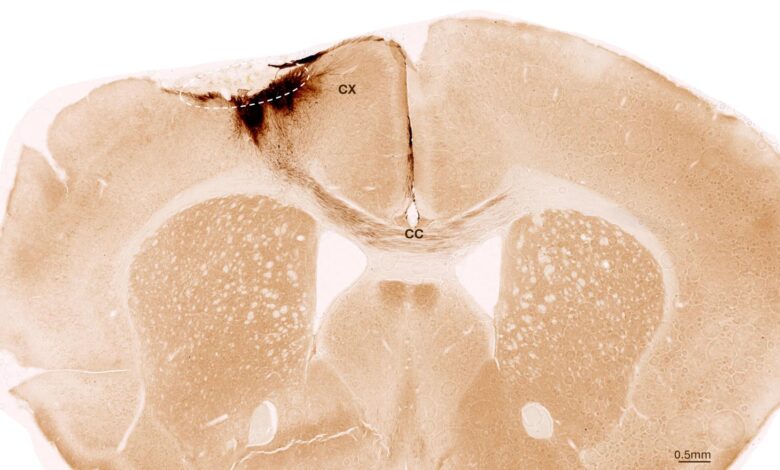
Terapie kmenové buňky zvrátila poškození mrtvice u myší, regenerující neurony a obnovování pohybu.
Tato zjištění přibližují vědci k lidskému ošetření, které by jednoho dne mohlo po poranění mozku transformovat zotavení.
Průlom při zotavení mrtvice pomocí kmenových buněk
Jeden ze čtyř dospělých trpí mrtvicí v jejich životě a ponechává asi polovinu z nich se zbytkovým poškozením, jako je ochrnutí nebo poškození řeči, protože vnitřní krvácení nebo nedostatek přívodu kyslíku zabíjí mozkové buňky nevratně. V současné době neexistují žádné terapie k opravě tohoto druhu poškození. „Proto je nezbytné sledovat nové terapeutické přístupy k potenciální regeneraci mozku po onemocněních nebo nehodách,“ říká Christian Tackenberg, vědecký vedoucí divize ve skupině neurodegenerace na University of Curych (UZH) pro regenerativní medicínu.
Neurální kmenové buňky mají potenciál regenerovat mozkovou tkáň, jako tým vedený Tackenbergem a postdoktorandským výzkumným pracovníkem Rebecca Weber nyní přesvědčivě prokázal ve dvou studiích, které byly provedeny ve spolupráci se skupinou vedenou Ruslanem Rustem z University of Southern California. „Naše zjištění ukazují, že nervové kmenové buňky nejen vytvářejí nové neurony, ale také vyvolávají další regenerační procesy,“ říká Tackenberg.
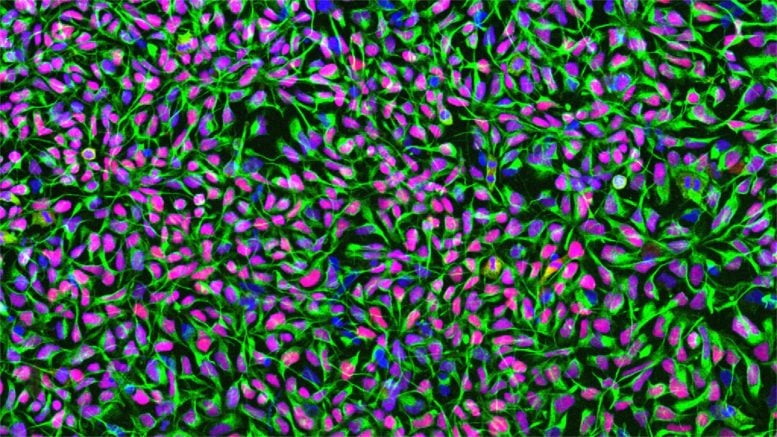
Nové neurony z lidských kmenových buněk
Studie používaly lidské nervové kmenové buňky, ze kterých se mohou tvořit různé typy buněk nervového systému. Kmenové buňky byly odvozeny z indukovaných pluripotentních kmenových buněk, které lze zase vyrobit z normálních lidských somatických buněk. Pro jejich zkoumání vědci vyvolali trvalou mrtvici u myší, jejichž charakteristiky se velmi podobají projevu mrtvice u lidí. Zvířata byla geneticky modifikována tak, aby neodmítla lidské kmenové buňky.
Jeden týden po indukci mrtvice výzkumný tým transplantoval nervové kmenové buňky do poškozené oblasti mozku a pozoroval následné vývoj pomocí různých zobrazovacích a biochemických metod. „Zjistili jsme, že kmenové buňky přežily po celou dobu analýzy po pěti týdnech a že většina z nich se transformovala na neurony, které dokonce dokonce komunikovaly s již existujícími mozkovými buňkami,“ říká Tackenberg.
Regenerace mozku mimo neurony
Vědci také našli další markery regenerace: nové tvorby krevních cév, útlum procesů zánětlivé reakce a zlepšenou integritu bariéry krve. „Naše analýza jde daleko nad rámec rozsahu dalších studií, které se zaměřily na okamžité účinky hned po transplantaci,“ vysvětluje Tackenberg. Naštěstí transplantace kmenových buněk u myší také zvrátila motorické poškození způsobené mrtvicí. Důkaz o tom byl částečně doručen analýzou myši s pomocí AI.
Klinická aplikace se přiblíží k realitě
Když navrhoval studie, Tackenberg již měl památky na klinické aplikace u lidí. Proto byly například kmenové buňky vyrobeny bez použití činidel odvozených od zvířat. Výzkumný tým založený na Curychu vyvinul pro tento účel definovaný protokol ve spolupráci s Centrem pro výzkum a aplikaci CIRA (CIRA) na Kjótské univerzitě. To je důležité pro potenciální terapeutické aplikace u lidí. Dalším objeveným pohledem bylo, že transplantace kmenových buněk funguje lépe, když se provádí ne okamžitě po mrtvici, ale o týden později, jak se ověřila druhá studie. V klinickém prostředí by toto časové okno mohlo výrazně usnadnit přípravu a implementaci terapie.
Výzvy, bezpečnostní opatření a budoucí výhled
Přes povzbudivé výsledky studií varuje Tackenberg, že stále existuje práce. „Musíme minimalizovat rizika a zjednodušit potenciální aplikaci u lidí,“ říká. Tackenbergova skupina opět ve spolupráci s Ruslanem Rustem v současné době pracuje na jakémkoli systému bezpečnostních přepínačů, který zabraňuje nekontrolovanému růstu kmenových buněk v mozku. Rovněž se také vyvíjí dodávka kmenových buněk endovaskulární injekcí, která by byla mnohem proveditelnější než mozkový štěp. Počáteční klinické studie využívající indukované kmenové buňky k léčbě Parkinsonovy choroby u lidí již v Japonsku probíhají, uvádí se hlásí Tackenberg. „Monda by mohla být jednou z dalších onemocnění, pro které je možné klinické hodnocení možné.“
Reference: “Neural Xenografts Contribute to Long-Term Recovery in Stroke via Molecular Graft-Host Crosstalk” by Rebecca Z. Weber, Beatriz Achón Buil, Nora H. Rentsch, Patrick Perron, Stefanie Halliday, Allison Bosworth, Mingzi Zhang, Kassandra Kisler, Chantal Bodenmann J. Zürcher, Daniela Uhr, Debora Meier, Siri L. Peter, Melanie Generali, Shuo Lin, Markus A. Rüegg, Roger M. Nitsch, Christian Tackenberg a Ruslan Rust, 16. září 2025, Přírodní komunikace.
Dva: 10.1038/S41467-025-63725-3
Nikdy nezmeškáte průlom: Připojte se k zpravodaji Scitechdaily.
Sledujte nás Google, Objevita Zprávy.