Vědci objevují podivné skryté struktury v DNA

Vědci zjistili, že kroucení struktur v DNA dlouho mylné za uzly jsou vlastně něco úplně jiného.
Uvnitř buněk, DNA Je zkroucena, zkopírována a roztažena. Zvraty mohou ovlivnit to, jak fungují geny, což ovlivňuje, které jsou zapnuté a kdy. Studium toho, jak DNA reaguje na stres, může vědcům pomoci lépe porozumět tomu, jak jsou geny kontrolovány, jak je organizována molekula a jak by problémy s těmito procesy mohly přispět k onemocnění.
Po celá léta vědci používají nanopory – malé díry dostatečně široké, aby se jeden řetězec DNA proklouzl – aby rychle a levně přečetl sekvence DNA. Tyto systémy fungují měřením elektrického proudu protékajícího nanoporem. Když prochází molekula DNA, narušuje to proud zřetelným způsobem, který odpovídá každému ze čtyř „písmen“, která tvoří kód DNA: A, T, C a G.
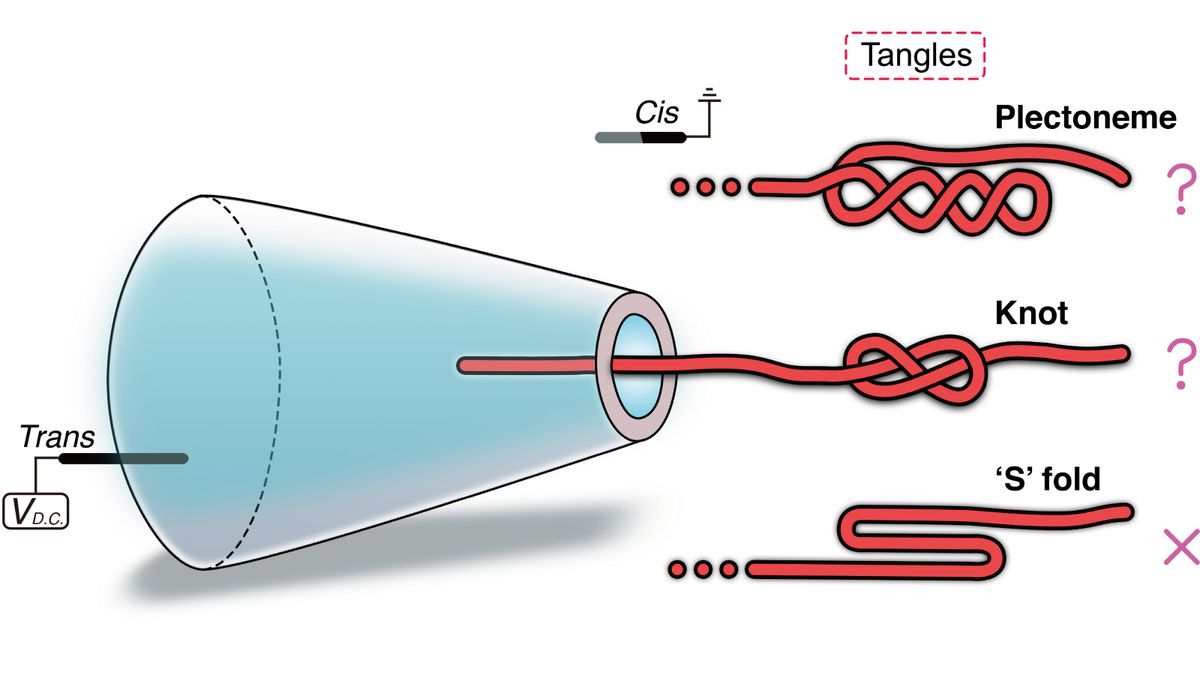
Neočekávané zpomalení nebo hroty v tomto signálu byly často interpretovány jako uzly v DNA. Nyní však nová studie zveřejněná 12. srpna v časopise Fyzikální recenze x Zjistí, že tyto změny signálu mohou také znamenat Plectonemes, což jsou přírodní cívky, které se tvoří, když se DNA krouží pod stresem.
„Uzly a plectonemy mohou vypadat velmi podobně v nanopore signálech,“ autor vedoucí studie Ulrich KeyserLIVE Science řekl, že fyzik na kavidské laboratoři University of Cambridge Laboratory. „Ale pocházejí z velmi odlišných fyzikálních mechanismů. U
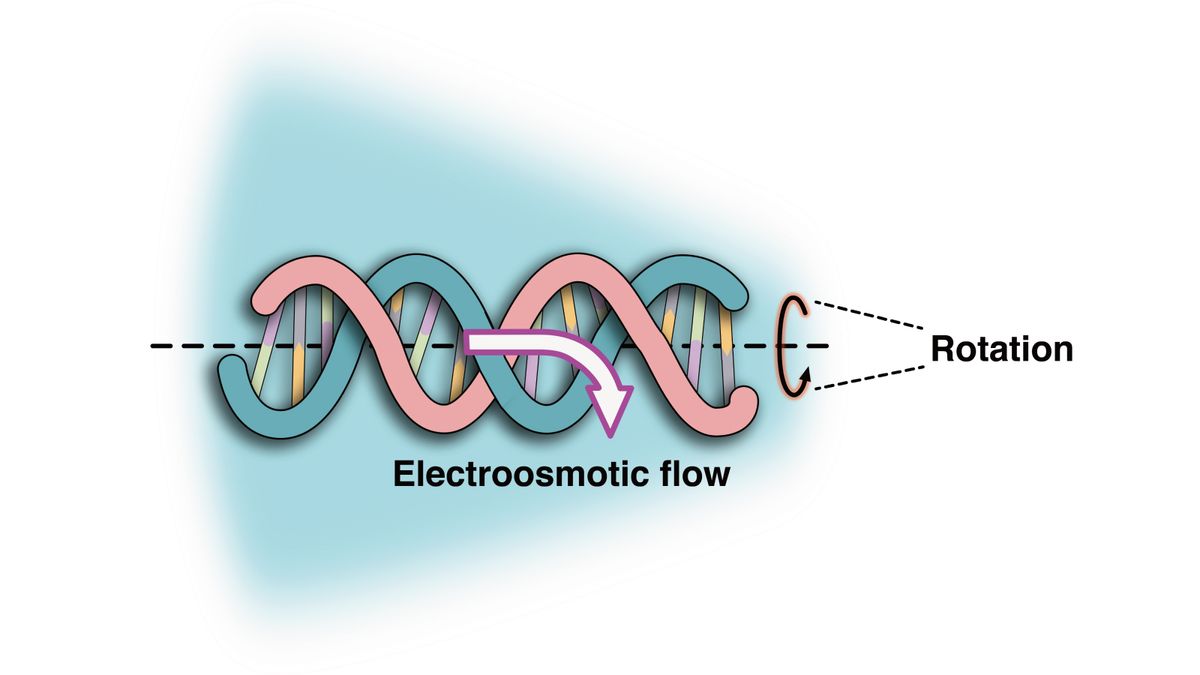
Aby studovali tyto cívky, vědci prošli pramenem DNA nanoporem ve tvaru kužele ve slaném roztoku s vysokým pH. Roztok pomohl vytvořit elektroosmotický tok, což znamená, že se DNA začala otáčet, když vstoupila do pórů. Pohyb generoval dostatečně silnou krouticí sílu nebo točivý moment, který stočil DNA, vysvětlil Keyser.
Keyser a jeho tým také aplikovali elektrické napětí napříč nanoporem, které pomáhají řídit DNA skrz a měřit změny v elektrickém proudu.
„V těchto druzích systémů nanočástic je vše velmi vysoké tření, takže DNA se pohybuje téměř jako by plavala medem,“ řekl Keyser. „Je to velmi viskózní prostředí, takže relativně vysoké síly tlačí DNA tímto pohybem vývrtky.“
Vědci analyzovali tisíce těchto událostí. Zatímco v experimentu se stále objevovaly některé uzly, měly tendenci být menší – přibližně 140 nanometrů napříč – zatímco Plectonémy byly asi 2 100 nanometrů napříč. Jakmile se napětí aplikované na systém zvýšilo, plekóné se staly běžnější díky silnějšímu točivému momentu.
Pro další testování toho, jak kroucení ovlivňuje chování DNA, vědci zavedli malé přestávky, zvané Nicks, do jednoho pramene dvojité šroubovice DNA. Tyto přezdívky umožnily snadnější otáčení DNA a uvolňování napětí, které zase způsobilo, že se vytvořilo méně plekóné. To potvrdilo, že torzní napětí je klíčovým hnacím motorem formace těchto struktur.
„Když jsme ovládali schopnost molekuly otáčet, mohli bychom změnit, jak často se objevily Plectonesmes,“ řekl Keyser.
Ačkoli jsou nanopory velmi odlišné od živých buněk, tyto druhy plectonemů se mohou také tvořit během procesů, jako je transkripce a replikace DNA. Transkripce popisuje, když se kód DNA zkopíruje jinou molekulou, volanou RNAa odesláno do buňky. Replikace popisuje, když je molekula DNA replikována plně, což se děje, když se například dělí buňka.
„Věřím, že torze v molekulách může ve skutečnosti vést k vytvoření i-motivů a G-kvadruplexy„Keyser řekl Live Science a dával jména dvou konkrétních typů uzlů, které jsou vidět v DNA. Takže to, co našli ve své laboratorní studii, má pravděpodobně důsledky pro živé buňky, vysvětlil.
Keyser a jeho tým zkoumají, jak se vytvářejí plectonemy a další struktury DNA během přírodních procesů, jako je transkripce. V dřívější práceZkoumali, jak torzní stres ovlivňuje replikaci DNA. Nanopory dávají vědcům způsob, jak nejen číst DNA, ale také sledovat, jak se chová, tato studie zdůrazňuje.
„Jen skutečnost, že molekula DNA může vytlačit póry, kde má být jeho tuhost mnohem větší než průměr pórů, je docela úžasná,“ Slaven GarajLIVE Science řekl fyzik na Národní univerzitě v Singapuru, který nebyl součástí studie. „Je to 10, 50, dokonce 100krát tužší než velikost pórů. Stále se ohýbá a prochází.“
Garaj byl nadšení z těchto zjištění. V budoucnu „bychom mohli být schopni oddělit torze vyvolanou nanopore od torze, která již byla v DNA dříve. To by nám mohlo nechat prozkoumat přirozené supercoring novým způsobem,“ dodal. To by bylo důležité pro pochopení toho, jak cívky a uzly kontrolují genovou aktivitu.