Vědci odhalí nové vodítko uvnitř elektrárny

Vědci Rockefeller zjistili, že antioxidační glutathion, působící v mitochondriích, hraje klíčovou roli při umožnění šíření nádorů prsu do plic.
Mitochondrie jsou nejlépe známé jako Powerhouse Cell, ale rostoucí důkazy naznačují, že také hrají ústřední roli při řízení rakoviny. Nový výzkum identifikoval mitochondriální metabolit glutathion jako klíčový faktor, který umožňuje buňkám rakoviny prsu oddělit se od primárního nádoru, šířit se tělem a etablovat se v nových tkáních.
Zjištění patří mezi první, kdo spojuje specifický mitochondriální metabolit s metastázami se silnými důsledky pro studium rakoviny na buněčné úrovni. „Doufáme, že naše práce upozorní na to, jak jsou organely a jejich metabolity relevantní pro biologii rakoviny,“ říká Kivanç Birsoy, vedoucí laboratoře metabolické regulace a genetiky v Rockefelleru.
Záhadné spojení s metastázami
Většina úmrtí na rakovinu nedochází ne kvůli původnímu nádoru, ale kvůli šíření nemoci. Protože metastázy jsou hlavní příčinou úmrtnosti na rakovinu, vědci se dlouho snažili odhalit mechanismy, které umožňují rakovinným buňkám osvobodit se od jejich primárního místa a kolonizovat vzdálené orgány.
Předchozí studie ukázaly, že metabolity, jako je laktát, pyruvát, glutamin a serin, přispívají do různých fází metastáz. Protože mitochondrie nejen produkují buněčnou energii, ale také vytvářejí metabolity, není divu, že nedávná práce svázala mitochondriální aktivitu s šířením rakoviny prsu, ledvin a pankreatu.
Přesné molekulární hráče však zůstaly nejasné. „Mitochondrie mají tisíce metabolitů a bylo obtížné určit, které jsou důležité pro tvorbu a růst nádoru a které iniciují metastázy,“ vysvětluje Birsoy.
Buňky pod stresem
K vyřešení této otázky použil Birsoy a jeho kolegové přístup k značení proteinů, který jim umožnil rozlišovat mezi buňkami, které zůstaly v nádoru prsu, a budovami, které se šířily do plic. Tým, vedený postgraduálním kolegou Nicole Delgaudio a postdoktorandským kolegou HSI-Wen Yeh, pak zkoumal, jak se metabolitové složení mitochondrií změnilo, když se rakovinné buňky etablovaly v nových tkáních.
„Tyto techniky nám umožnily nestranným způsobem vidět rozdíl mezi tím, co je nezbytné v metastázách a tím, co je nezbytné v primárním nádoru,“ říká Delgaudio.
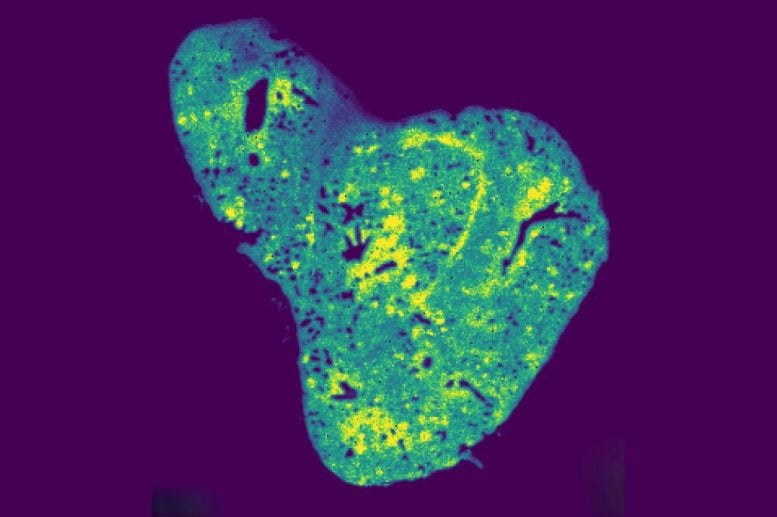
Z tisíců mitochondriálních metabolitů se glutathion objevil jako výrazný kandidát. Tento antioxidant, známý pro snižování oxidačního stresu, napomáhající detoxikaci a podporu imunitní funkce, byl nalezen ve prudce zvýšených hladinách v metastatických rakovinných buňkách, které dosáhly plic. Pro ověření pozorování vědci použili prostorovou metabolomiku k přímému vizualizaci distribuce glutathionu v plicních tkáních.
Zkoumání se poté posunulo směrem k mitochondriální membránové proteiny. Screening odhalil, že jeden vynikl jako nepostradatelný pro metastatické rakovinné buňky: SLC25A39, transportér, který importuje glutathion do mitochondrií. Společně zjištění zjistila přímé spojení mezi glutathionem a jeho transportérem, což ukazuje, že mitochondriální glutathion import prostřednictvím SLC25A39 je kritickým hnacím motorem metastázy rakoviny.
Birsoy a jeho kolegové také zjistili, jak mitochondriální glutathion řídí šíření rakoviny: ne působením jako antioxidant-účinek vyloučil prostřednictvím několika experimentů-ale signalizací pro aktivaci ATF4, transkripční faktor, který pomáhá rakovinným buňkám přežít v podmínkách s nízkým oxygenem. To také určilo, když je glutathion specificky vyžadován: během časných kroků metastatické kolonizace, když se rakovinné buňky rychle přizpůsobují stresujícímu prostředí nové tkáně.
Známý viník
Tato práce staví Nedávná významná práce Z laboratoře Birsoy. V roce 2021 byl jeho tým první, kdo prokázal, že SLC25A39 je transportér, který přináší glutathionu do mitochondrií; V roce 2023 ukázali, že SLC25A39 není jen transportér, ale dynamický senzor, který reguluje množství glutathionu v mitochondriích a podle toho upravuje tyto úrovně. Když se tedy tento metabolit a jeho mitochondriální transportér objevil v screeningu rakoviny, Birsoy věděl, kam přijmout jeho experimenty dál.
„Protože jsme tento transportér našli dříve a věděli jsme, jak blokovat vstup glutathionu, již jsme měli nástroje nezbytné k prozkoumání jeho role v metastázování rakoviny,“ říká.
Tato zjištění mohou mít klinické důsledky – zejména proto, že tým také zjistil, že vzorky rakoviny prsu od pacientů, jejichž onemocnění se rozšířilo do plic, vykazovaly zvýšenou SLC25A39 a že vyšší exprese SLC25A39 byla silně korelována s horším celkovým přežitím u pacientů s rakovinou prsu. Jednoho dne by malá molekula, která se zaměřuje na tento metabolit blokováním jeho transportéru, by mohla potenciálně zabránit metastázům rakoviny prsu, s menším počtem vedlejších účinků než zametání terapií, které se zaměřují na obecnější buněčné procesy.
V krátkodobém horizontu však článek zdůrazňuje důležitost přibití, jak metabolity v různých kompartmentech fungují v našich buňkách.
„Snažíme se zvýšit přesnější znalosti metabolismu,“ říká Birsoy. „Nejde jen o to, aby se stoupaly některé úrovně metabolitů a jiní klesají. Musíme se podívat na organely, přesné kompartmenty, abychom pochopili, jak metabolity ovlivňují lidské zdraví.“
Reference: „import mitochondriálního glutathionu umožňuje metastázy rakoviny prsu prostřednictvím integrované signalizace stresové odezvy“ od HSI-Wen Yeh, Nicole Lauren. Delgaudio, Beste Uygur, Alon Millet, Artem Khan, Gokhan Unlu, Michael Xiao, Rebecca C. Timson, Caifan Li, Kerem Ozcan, Karl W. Smith, Luiza Martins. Nascentes Melo, Gabriele Allies, Olca Basturk, Albert Sickmann, Erol C. Bayraktar, Richard Possemato, Alpaslan Tasdogan a Kivanc Birsoy, 31. července 2025, Objev rakoviny.
Dva: 10.1158/2159-8290.CD-24-1556
Nikdy nezmeškáte průlom: Připojte se k zpravodaji Scitechdaily.