Epigenetické přeprogramování bezpečně modifikuje více genů v T buňkách současně pro CAR-T terapie
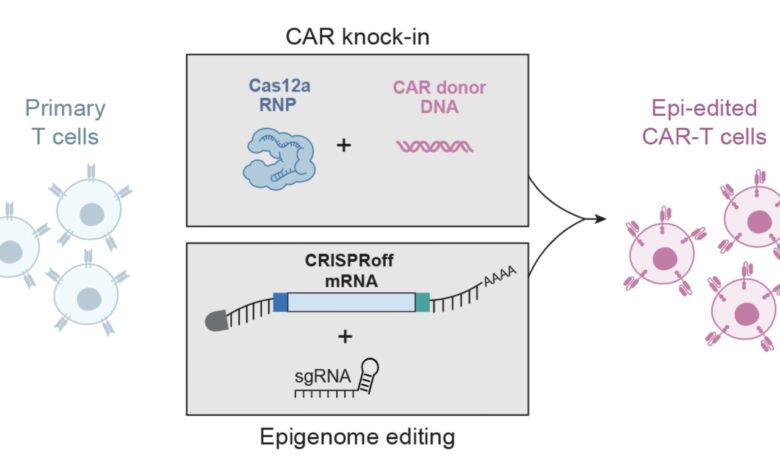
Primární T buňky modifikované pomocí dvou přístupů. Receptory CAR jsou zavedeny cílenou inzercí DNA (nahoře), zatímco mRNA CRISPRoff a vodicí RNA umlčují další geny prostřednictvím epigenetických modifikací (dole). To vytváří buňky CAR-T se zvýšenými schopnostmi bez toxicity řezání DNA na více místech. Kredit: Chiara Ricci-Tam
Arc Institute, Gladstone Institutes a University of California, San Francisco, vědci vyvinuli epigenetickou editační platformu, která umožňuje bezpečnou modifikaci více genů v primárních lidských T buňkách a řeší klíčový problém výroby a škálovatelnosti v buněčných terapiích nové generace.
Výzkum, publikovaný v Přírodní biotechnologiedemonstruje, jak CRISPRoff a CRISPRon mohou přeprogramovat pacientovy vlastní T buňky pro terapeutické účely bez buněčné toxicity a poškození DNA spojených s tradičními přístupy k úpravě genů.
Rostoucí počet terapií T-buněk, včetně intervencí CAR-T, jsou personalizovanou léčbou, která geneticky modifikuje pacientovy T-buňky tak, aby cílily a ničily rakovinné buňky. Tyto přístupy byly úspěšné proti rakovině krve, ale často selhávají při aplikaci na pevné nádory, které vytvářejí nepřátelské prostředí, které nadměrně stimuluje a následně vyčerpává T buňky.
Ukázalo se však, že použití CRISPR ke konstrukci složitějších „obrněných“ T-buněk, které mají energii k provozu v pevných nádorech, je náročné kvůli toxicitě a buněčná smrt způsobené úpravou několika genů současně.
CRISPRoff a CRISPRon se tomuto problému vyhýbají tím, že vědcům umožňují programově umlčet nebo aktivovat geny epigenetické modifikace– stabilní chemické značky, které řídí genovou expresi bez řezání DNA nebo změny genomové sekvence.
CRISPRoff umlčuje geny, které normálně omezují funkci T buněk, ukládáním methylačních značek na cílové promotory, zatímco CRISPRon aktivuje prospěšné geny odstraněním těchto značek.
Na rozdíl od tradičních přístupů CRISPR, které vyžadují řezání šroubovice DNA, což může poškodit nebo zabít T buňky, mohou tyto epigenetické editory modifikovat až pět genů současně při zachování vysoké míry přežití buněk.
„T buňky si v podstatě zapamatují naše programovací instrukce,“ říká Luke Gilbert, hlavní výzkumník Arc Institute a docent na UCSF.
„Epigenetické editory dodáváme jen pár dní, ale efekty umlčování genů zůstávají stabilní díky desítkám buněčných dělení a několika kolům imunitní aktivace.“
Aby vědci demonstrovali potenciál platformy, vytvořili vylepšené CAR-T buňky vložením receptorů cílených na rakovinu pomocí CRISPR a současným použitím CRISPRoff k umlčení RASA2, genu, který působí jako molekulární brzda aktivace T buněk.
Buňky s dvojitým inženýrstvím si udržely svou schopnost zabíjet rakovinu opakovanými testy v laboratorních testech, zatímco buňky CAR-T bez umlčení RASA2 se vyčerpaly. U myších modelů leukémie poskytly zesílené CAR-T buňky významně lepší kontrolu nádoru a lepší přežití ve srovnání se standardními přístupy CAR-T.
„Tady, používáme genetické inženýrství naprogramovat T buňky k hledání rakovinné buňky a pomocí epigenetického inženýrství naprogramovat sílu jejich protirakovinné funkce,“ říká Alex Marson, ředitel Gladstone-UCSF Institute of Genomic Immunology a spoluautor studie.
„Spojení kombinované síly genetického a epigenetického inženýrství nyní nabízí široké naděje na vývoj odlišných programů pro léčbu široké škály různých onemocnění.“
„Namísto pouhého přidávání schopností cílení můžeme systematicky přeprogramovat, jak tyto buňky fungují škálovatelným způsobem, abychom vytvořili účinnější terapeutické produkty,“ říká první autor Laine Goudy, Ph.D. student v laboratořích Marsona a Gilberta. „Údaje v tomto dokumentu by mohly podpořit přechod přímo do klinických studií pro určité aplikace.“
Kromě aplikací na rakovinu tento přístup otevírá nové možnosti pro léčbu autoimunitních onemocnění, transplantační medicínu a další oblasti, kde by přeprogramované T buňky mohly být přínosem pro pacienty.
CRISPRoff pracuje s protokoly výroby buněk, které se již používají k výrobě ošetření CAR-T schválených FDA, což vyžaduje pouze konverzi reagencií výzkumné kvality na verze klinické kvality. Výzkumný tým zvažuje další kroky pro testování technologie na lidech.
„Když jsme začínali, nebyli jsme si jisti, že to bude u T buněk úspěšné, a trvalo roky metodické optimalizace, než jsme překonali některé zásadní problémy, ale bylo tak potěšující vidět, že základní technologie je extrémně robustní,“ říká Gilbert. „Terapie CAR-T jsou neuvěřitelným úspěchem, ale v kontextu solidní nádoryvěříme, že náš přístup by mohl podpořit další generaci přístupů CAR-T ve prospěch pacientů.“
Gilbert je jedním ze čtyř vedoucích autorů tohoto článku, spolu s Brianem Shym, odborným asistentem na katedře laboratorní medicíny UCSF a ředitelem programu UCSF Investigational Cell Therapy Program, Justinem Eyquemem, docentem na Katedře mikrobiologie a imunologie UCSF, a Marsonem, který je také vedoucím výzkumníkem a profesorem na GUCladstone.SF.
Goudy vedl technický vývoj.
Další informace:
Integrované epigenetické a genetické programování primárních lidských T buněk, Přírodní biotechnologie (2025). DOI: 10.1038/s41587-025-02856-w.
Poskytuje
Arc Institute
Citace: Epigenetické přeprogramování bezpečně modifikuje více genů v T buňkách současně pro terapie CAR-T (2025, 21. října) získané 21. října 2025 z https://medicalxpress.com/news/2025-10-epigenetic-reprogramming-safely-multiple-genes.html
Tento dokument podléhá autorským právům. Kromě jakéhokoli poctivého jednání za účelem soukromého studia nebo výzkumu nesmí být žádná část reprodukována bez písemného souhlasu. Obsah je poskytován pouze pro informační účely.




