Vědci najdou způsob, jak „neprůstřelné“ T buňky proti rakovině
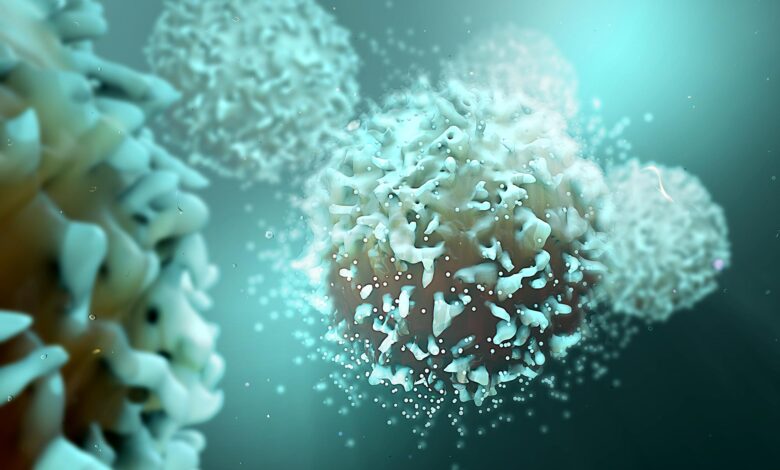
Poškození telomer řídí vyčerpání T buněk. Antioxidanty obnovily sílu boje proti rakovině u myší.
Nádorové prostředí kladou silný stres na imunitní buňky, které bojují proti rakovině. Omezený kyslík, zvýšená kyselost a další drsné podmínky přetížení mitochondrií, výrobci energie buněk, což přispívá k únavě T buněk a zhoršuje výsledky rakoviny.
Nová studie v Imunitavedené vědci v University of PittsburghU myší ukázali, že tyto podmínky vyzývají mitochondrie k uvolnění reaktivního kyslíku druh (ROS). Tyto molekuly cestují do jádra a poškozují telomery, což nakonec tlačí T buňky do nefunkčního stavu.
„Opravdu vzrušující část tohoto výzkumu je, že zabráněním poškození telomerů prostřednictvím cíleného antioxidantu můžeme zachránit funkci T buněk,“ řekla hlavní autorka Dayana Rivadeneira, docentka v Pitt Department of Imunology a UPMC Hillman Cancer Center. „Tím se otevírá dveře novým terapiím, aby se zlepšila účinnost imunoterapií rakoviny.“
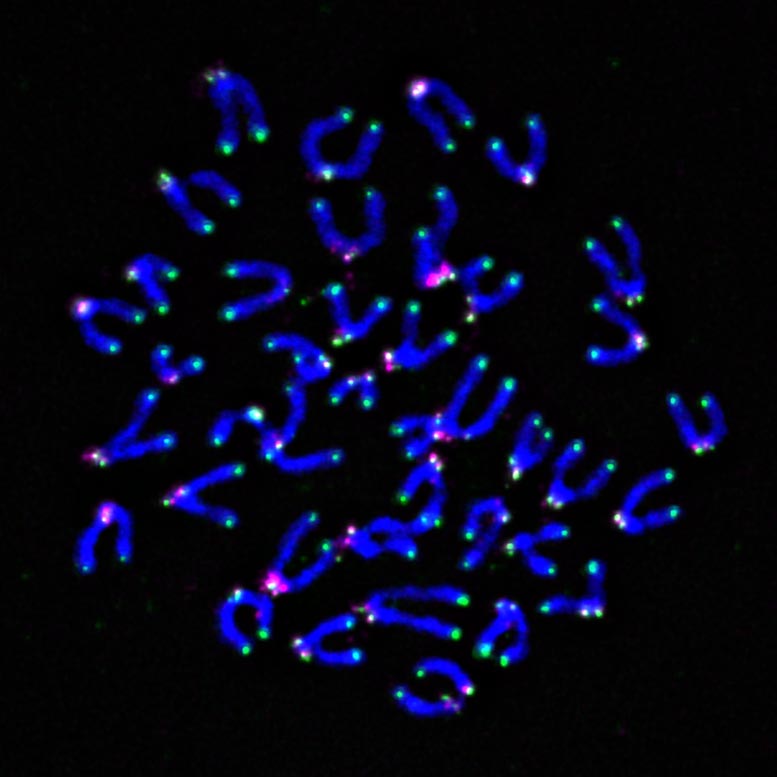
Neočekávané mitochondriální spojení
Rivadeneira a vedoucí autor Greg Delgoffe, profesor Pitt Department of Imunology a UPMC Hillman, původně neplánovali prozkoumat Telomery. Jejich počáteční zaměření bylo na to, jak mitochondriální poškození ovlivňuje výkon T buněk. Spolupráce s Patricií Opresko, profesorkou na Pitt Department of Pharmacology and Chemical Biology, a pozdní Marcel Bruchez, profesor biologických věd a chemie na Carnegie Mellon University, rozšířil studii tak, aby zahrnoval poškození telomerického.

Chcete-li to prozkoumat, týmové myší s genetickým systémem, který způsobuje vysoce lokalizované oxidační poškození v telomerech nebo mitochondriích, když je vystaven krajně červenému světlu.
„To, co jsme zjistili, bylo pozoruhodné,“ řekl Delgoffe. „Ať už jsme poškodili mitochondrie nebo telomery, dostali jsme stejný výsledek: nefunkční T buňky. Mezi motorem buňky a mozkem buňky, mitochondrií a jádrem, jsme dostali přeslech.“
„Když poškodíte mitochondrie, jednou z prvních věcí, která se poškozuje, jsou Telomery,“ dodala Rivadeneira. „A podobně, když poškodíte Telomery, mluví zpět s mitochondrií, aby zahájili program, který řekne buňce, aby se vypnula a byla vyčerpaná.“
Antioxidační terapie pro obnovení funkce
Protože ROS-vysoce reaktivní molekuly kyslíku, které způsobují poškození buněk-byly zodpovědné za telomerické poškození, Delgoffe a Rivadeneira předpokládali, že antioxidanty neutralizující ROS mohou chránit nebo obnovit funkci T buněk.
Aby neutralizovali ROS konkrétně v telomerech, vzali myší T buňky a přivázali antioxidační protein k jinému proteinu, který sídlí v Telomerech. Když tyto T buňky napadly do myší s agresivní formou melanomu, zvířata měla mnohem lepší přežití a menší nádory než ty, které byly podávány pravidelné T buňky.
Potenciál pro terapii CAR-T
Podle vědců by tento antioxidační přístup mohl být aplikován na CAR-T terapii, která zahrnuje vzít pacientovy T buňky a geneticky je inženýrství, aby lépe rozpoznaly rakovinné buňky před jejich oživením.
„Tento výzkum je vysoce překladatelný, protože tento přístup lze snadno začlenit do standardního protokolu CAR-T,“ řekl Delgoffe. „I když jste geneticky inženýrskými T buňkami, abyste zlepšili schopnost boje proti rakovině, můžete je také učinit neprůstřelnými proti oxidačnímu poškození.“
Nyní vědci pracují na vývoji podobného telomerově specifického antioxidačního přístupu pro modifikaci lidských T buněk, které nakonec doufají, že v klinických studiích testují.
Ve své nově spuštěné laboratoři plánuje Rivadeneira také prozkoumat, jak Telomere Health ovlivňuje imunitní systém a výsledky rakoviny. Jednou z oblastí zájmu je pochopení toho, jak chemoterapie mění funkci T buněk poškozením telomerů a zda by to mohlo ovlivnit, zda pacienti reagují na imunoterapii.
Reference: „Nestabilita telomery vyvolaná oxidačním stresem řídí dysfunkci T buněk u rakoviny“ od Dayana B. rivadeneira, Sanjana Thosar, Kevin Quann, William G. Gunn, Victoria G. Dean, Bingxian Xie, Angelina Parise, Andrew C. McGovern, Kellie Spahr, Konstantinos Lyan P. bars, Marcel P. bars, Marcel P. Barnez, Marcel P. Bresin, Marcel P. Bresion, Marcel P. Bresion, Marcel P. Bresion, Marcel P. Bresion, Marcel P. Bresion, Marcel P. Patricia L. Opresko a Greg M. Delgoffe, 9. září 2025, Imunita.
Doi: 10.1016/j.immune.2025.08.008
Financování: NIH/Národní zdravotní ústavyInstitut pro výzkum rakoviny, Mark Foundation for Cancer Research
Nikdy nezmeškáte průlom: Připojte se k zpravodaji Scitechdaily.




