Rakovinné buňky s nedostatkem MTAP sdílejí signály, které umlčují imunitu
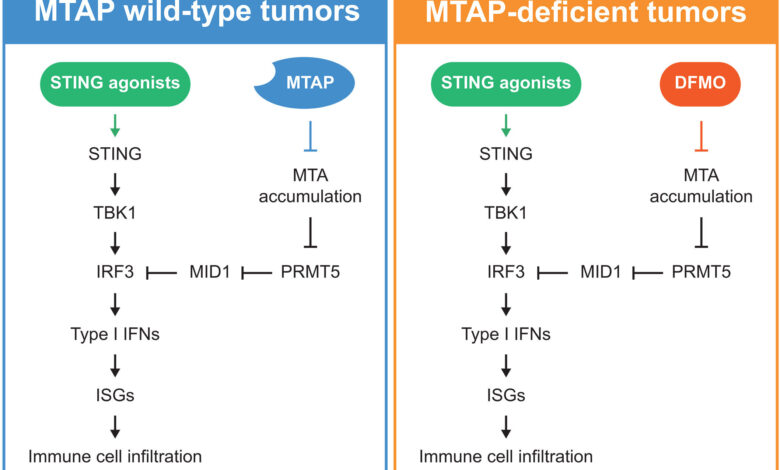
MTAP-dependentní regulace dráhy STING a terapeutická strategie s agonisty STING. Kredit: Věda (2025). DOI: 10.1126/science.adl4089
Čínská lékařská univerzita vede multiinstitucionální tým, který uvádí, že nedostatek MTAP potlačuje snímání cytosolových nukleových kyselin a zvyšuje odolnost vůči agonistům STING, přičemž existující lék, DFMO, obnovuje aktivitu dráhy a protinádorové reakce.
MTAP kóduje methylthioadenosin fosforylázu, enzym v methioninové záchranné cestě, která recykluje methylthioadenosin na methionin. Gen sídlí na chromozomu 9p21.3, sousedícím s tumor supresorové geny CDKN2A a CDKN2B a je s nimi často společně deleován u různých lidských rakovin. Ztráta MTAP byla spojena se změněným buněčným metabolismem a změnami v metylačních drahách, ale jeho širší účinky na imunitní signalizaci zůstávají předmětem zkoumání.
Difluormethylornithin (DFMO) byl původně vyvinut v 70. letech minulého století k léčbě parazitárních infekcí. Přestože od té doby zaznamenal řadu aplikací, předklinické studie ukázaly, že DFMO snižuje koncentrace polyaminů a zpomaluje proliferaci nádorových buněk na zvířecích modelech tlustého střeva, prsu a rakovina prostaty. Příznivý bezpečnostní profil DFMO a jeho mechanismus inhibice polyaminové dráhy vedly k jeho zkoumání u jiných typů nádorů a strategií kombinované imunoterapie.
Cytosolické dráhy snímání nukleových kyselin jsou cíli pro přeměnu imunitních pouštních nádorů na imunoaktivní nádory a předchozí studie na zvířatech s agonisty STING ukázaly silnou protinádorovou aktivitu, zatímco studie na pacientech neuváděly žádný zjevný přínos, což naznačuje translační mezeru.
Ve studii „nedostatek MTAP propůjčuje rezistenci vůči cytosolickému snímání nukleových kyselin a agonistům STING,“ zveřejněno v Vědavýzkumníci navrhli řadu molekulárních a in vivo experimentů, aby zjistili, jak ztráta MTAP mění signalizaci interferonu a zda cílení na metabolismus polyaminu pomocí DFMO může obnovit aktivitu dráhy a protinádorové reakce.
Výzkumníci použili izogenní páry lidských rakovinných buněčných linií, které se liší pouze stavem MTAP, tkáňové mikročipy ze 430 vzorků nádorů pro korelaci MTAP–IRF3 a bilaterální syngenní myší modely využívající nádory EMT6 a MC38 u myší BALB/c a C57BL/6.
Ztráta MTAP ztlumila základní alarm nebezpečí uvnitř rakovinné buňky. Napříč isogenními páry vykazovaly buňky postrádající MTAP slabé vzplanutí genů stimulovaných IFNβ a interferonem po poly(dA:dT), poly(I:C) nebo 2ʹ,3ʹ-cGAMP. Opětovné přidání MTAP nebo IRF3 tyto signály obnovilo. Lidské nádory vykazovaly stejný vztah. Tkáňové mikročipy ze 430 vzorků imunohistochemicky propojily vyšší MTAP s vyšším proteinem IRF3.
Mechanistická práce sledovala řetězec od metabolismu k imunitní signalizaci. Ztráta MTAP způsobila nahromadění methylthioadenosinu, který inhiboval PRMT5, snížil protein IRF3 a otupil snímání cytosolové nukleové kyseliny. Experimenty s podmíněným středním výkonem a přímá léčba methylthioadenosinem rozšířily tuto brzdu na sousední MTAP-intaktní rakovinu a imunitní buňkysnížení aktivity PRMT5 a IRF3 u těchto sousedů.
Studie transkriptů a proteinů konvergovaly spíše k regulované degradaci než ke ztrátě transkripce. RNA-seq nevykazovala konzistentní pokles mRNA IRF3, zatímco MID1 se zvýšil s knockoutem MTAP, knockdown PRMT5 nebo inhibicí PRMT5. Blokování proteazomu obnovilo IRF3 v MTAP-deficientních buňkách. Sražení MID1 obnovilo IRF3. Vynucení exprese MID1 stlačilo IRF3 dolů v MTAP-intaktních buňkách.
DFMO zvrátilo metabolické úzké hrdlo a oživilo snímání. Léčba snížila methylthioadenosin, obnovila aktivitu PRMT5, snížila MID1 a zachránila IRF3 spolu s IFNp a interferonem stimulovanými geny v MTAP-deficientních a MTAP-nulových buňkách.
Studie na myších odrážely buněčná data. Nádory postrádající MTAP odolávaly agonistům STING. Spárování DFMO s agonistou STING zmenšilo nádory na injekčních a vzdálených bocích a zlepšilo přežití v modelech EMT6 a MC38 se zvýšeným CD4+ T buňky, CD8+ T buňky, dendritické buňky a B buňky uvnitř nádorů.
Průzkumy genomu rakoviny mapovaly klinické pozadí. Inaktivace MTAP se objevila u asi 11 % nádorů, inaktivace STING asi u 27 % a obě dohromady asi u 2 %, což ukazuje na do značné míry oddělené skupiny.
Autoři dospěli k závěru, že stav MTAP může vést k třídění pacientů pro imunoterapii založenou na STING a že DFMO by mohl zvýšit klinickou účinnost agonistů STING u nádorů s delecí MTAP.
Napsal pro vás náš autor Justin Jacksonupravil Gaby Clarkováa fakta ověřena a zkontrolována Robert Egan—tento článek je výsledkem pečlivé lidské práce. Spoléháme na čtenáře, jako jste vy, že udrží nezávislou vědeckou žurnalistiku při životě. Pokud je pro vás toto hlášení důležité, zvažte prosím a dar (zejména měsíčně). Dostanete bez reklam účet jako poděkování.
Další informace:
Jung-Mao Hsu et al, nedostatek MTAP propůjčuje rezistenci vůči cytosolickému snímání nukleové kyseliny a agonistům STING, Věda (2025). DOI: 10.1126/science.adl4089
© 2025 Science X Network
Citace: Rakovinové buňky s deficitem MTAP sdílejí signály, které umlčují imunitu (2025, 22. října) získané 22. října 2025 z https://medicalxpress.com/news/2025-10-mtap-deficient-cancer-cells-silence.html
Tento dokument podléhá autorským právům. Kromě jakéhokoli poctivého jednání za účelem soukromého studia nebo výzkumu nesmí být žádná část reprodukována bez písemného souhlasu. Obsah je poskytován pouze pro informační účely.




