Zebrafish model pro ultrarasené genetické onemocnění odhaluje dva slibné kandidáty na drogy
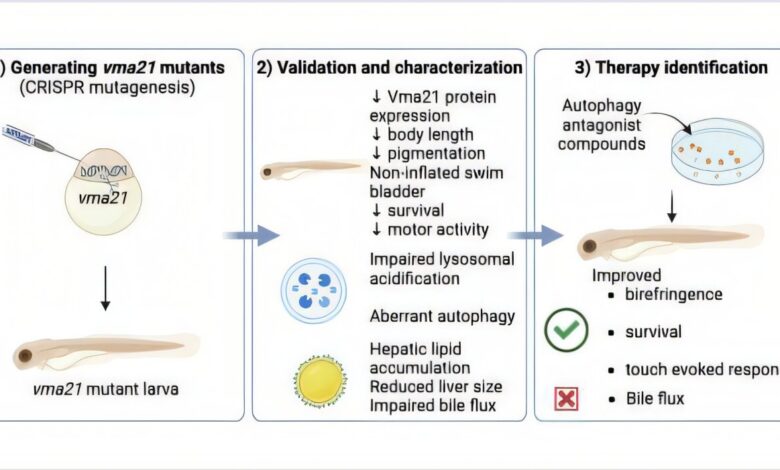
Kredit: Molekulární medicína EMBO (2025). Dva: 10.1038/S44321-025-00204-8
Může malá ryba pomoci identifikovat možné ošetření u velmi vzácné zděděné nemoci nalezené u chlapce v Alabamě? Genetické onemocnění je XMEA, což postupně oslabuje svaly a může ovlivnit játra a srdce. XMEA znamená myopatii vázanou na X s nadměrnou autofagií. Od března 2024 bylo po celém světě viděno pouze 33 případů.
Po DNA sekvenci chlapeckého genomu ukázala mutaci v genu VMA21, jednu ze známých příčin XMEA, University of Alabama v Birminghamu a dětským dětským neurologem Alabama Michael Lopez, MD, Ph.D., postoupila rodině UAB centra pro přesné modelování zvířat nebo C-PAM.
V C-PAM a ve spolupráci s kanadskou skupinou, výzkum vedený Matthew Alexander, Ph.D., UAB Department of Pediatrics, Division of Pediatric Neurology a Jim Dowling, MD, Ph.D., nemocnice pro nemocné děti, Toronto, Ontario, vytvořil preklinický model XMEA v Zebrafish the Analogous, který je analogy pro VMA21.
Zatímco tato malá, pruhovaná ryba se běžně vyskytuje v domácích akváriích, zebrafish jsou také cenným zvířecím modelem pro lidské onemocnění kvůli rychlý růstVelké velikosti spojky a snadná genetická manipulace. Jsou také transparentní jako larvy.
V a Studie zveřejněna v Molekulární medicína EMBOAlexander a Dowling nyní ukazují, že jejich mutantní zebrafish oslabil svaly a další příznaky, které odrážejí lidskou nemoc XMEA. U tohoto jednoduchého modelu dokázali testovat 30 klinicky testovaných léčiv a identifikovat dva, které významně zlepšily příznaky XMEA u zebrafish. Nyní studují mutaci VMA21 v savčím modelu, myši, aby dále posunuli výzkum k možné klinické léčbě.
„Zřídili jsme první předklinický zvířecí model XMEA a zjistili jsme, že tento model věrně rekapituluje většinu rysů lidské choroby,“ řekl Alexander. „Je tedy ideální pro stanovení patomechanismů onemocnění a identifikaci terapií.“
Vědci použili CRISPR-Cas9, často nazývaní molekulární nůžky pro DNA, k vytvoření dvou mutantů: mutace rámce způsobená delecí proteinu s jednou základnou a předčasným stopkovým kodonem vytvořeným během delece 14 párů bází a vložení 21. obou mutací ztráty funkce VMA21.
Oba mutanty vykazovaly změny v souladu se změněnou strukturou a funkcí svalové struktury, jako je kratší délka těla a neplavené plavecké měchýře. Měli sníženou schopnost plavat se od podnětu a strávili méně času plaváním a ve srovnání se zebrafish divokého typu cestovali menší vzdáleností.
Klíčovou změnou buněk v lidském XMEA je zhoršení autofagie, recyklačního systému buňky. Autofagie se odehrává v buněčných organelách zvaných lysosomy a ty musí být kyselé, aby aktivovaly proteázy, které degradují proteiny pro recyklaci do nových proteinů. Stejně jako lidské XMEA i mutantní rybí lysozomy vykazovaly selhání při okyselení a svalové buňky měly charakteristické vakuoly-uzavřené struktury naplněné pochvalu. Stejně jako pacienti s lidmi XMEA i ryby vykazovaly patologie jater a srdce.
Na rozdíl od lidského XMEA, která se může lišit od mírných po střední příznaky jako progresivní onemocnění, mutantní ryby vykazovaly závažné snížení v in životnostpravděpodobně kvůli úplnější ztrátě funkce VMA ve srovnání s lidskými pacienty.
Protože ryby narušily autofagii a protože pro pacienty XMEA neexistují žádné terapie, vědci testovali 30 klinicky testovaných autofagických inhibičních sloučenin z knihovny léků Selleckchem na rybách XMEA.
Screening spojků pro změněnou svalovou birefringenci, změna v lomu polarizovaného světla, která naznačuje sníženou organizaci svalů, tým identifikoval devět sloučenin, které jak snížily abnormální dvojlom, tak prodloužené přežití ryb. Dlouhodobé testování devíti pro zlepšení přežití a plavání ukázalo, že Edaravon a LY294002 měly největší terapeutické účinky.
„Vzrušeně jsme zjistili, že několik antagonistů autofagie by mohlo zlepšit aspekty fenotypu zebrafish VMA21 a zejména dvě sloučeniny zlepšily fenotyp napříč více doménami dvojnásobné, motorové funkce a přežití,“ řekl Alexander. „Skutečnost, že mnohonásobné modulátory autofagie zmírnily aspekty fenotypu, podporuje důležitou roli autofagie v procesu onemocnění a propůjčuje důvěru platnosti a potenciální překladatelnosti nálezů na pacienty.“
Spoluautory s Alexanderem a Dowlingem ve studii jsou Lily Huang, Rebecca Simonian a Lacramioara Fabian, nemocnice pro nemocné děti; a Michael A. Lopez, Muthukumar Karuppasamy, Veronica M. Sanders a Katherine G. English, UAB Department of Pediatrics, Division of Pediatric Neurology.
Více informací:
Lily Huang et al, X-vázaná myopatie s nadměrnou autofagií: charakterizace a testování terapie v modelu zebrafish,, Molekulární medicína EMBO (2025). Dva: 10.1038/S44321-025-00204-8
Poskytnuto
University of Alabama v Birminghamu
Citace: Zebrafish model pro ultrarasené genetické onemocnění odhaluje dva slibné kandidáty na léky (2025, 5. června) získané 5. června 2025 z https://medicalxpress.com/news/2025-06-Ebrafish-ultra-rare-genetic-desease.
Tento dokument podléhá autorským právům. Kromě jakéhokoli spravedlivého jednání za účelem soukromého studia nebo výzkumu nemůže být žádná část bez písemného povolení reprodukována. Obsah je poskytován pouze pro informační účely.




